题目内容
【题目】20℃时,根据某固体在不同质量的水中达饱和时溶解的质量绘成如图斜线,有关说法错误的是
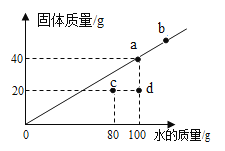
A. 20℃时,该物质的溶解度为40g
B. d→a点可以增加溶质或蒸发溶剂
C. a点对应的溶液降温不一定有晶体析出
D. b与c点对应溶液的溶质质量分数关系是:c<b
【答案】B
【解析】
A、根据图示可知,20℃时,该物质在100g水中溶解40g达到饱和状态,该物质在的溶解度为40g,故A正确;
B、d→a溶剂的质量不改变为100g,所以不能通过蒸发溶剂实现,故B错误;
C、该图示是溶剂和溶质的质量,没有温度的信息,不能得出该物质的溶解度随温度的升高而增大,a点对应的溶液降温不一定有晶体析出,故C正确;
D、c中有80g水,溶质是20g,c表示的溶液为该温度的不饱和溶液, b在曲线上,属于该温度下的饱和溶液,在同一温度,同一溶质饱和溶液的质量分数最大,b与c点对应溶液的溶质质量分数关系是:c<b,故D正确。故选B。

 新题型全程检测期末冲刺100分系列答案
新题型全程检测期末冲刺100分系列答案【题目】我国西北地区有很多咸水湖,其中最大的是柴达木盆地的察尔汗盐池。某盐湖附近的农民通过“冬天捞碱,夏天晒盐”获得大量湖盐。小伟同学取该湖盐样品进行探究。
(提出问题)该湖盐样品的成分是什么?
(查阅资料)冬天捞碱的“碱”指Na2CO3,夏天晒盐的“盐”指NaCl。
(猜想与假设)猜想一:Na2CO3
猜想二:NaCl
猜想三:Na2CO3和NaCl
(实验探究)
实验 | 实验操作 | 实验现象 | 实验结论 |
实验一 | 取少量样品于试管中,加适量水溶解后,加入过量稀HNO3 | 产生能使澄清石灰水变浑浊的气体 | ①猜想_____不成立 |
实验二 | ②向实验一所得的溶液中加入适量的_____ | ③_____ | 猜想三成立 |
(拓展延伸)为进一步确定该湖盐样品中Na2CO3的质量分数,小伟同学再取该湖盐样品10.00g做了如图1所示的补充实验。
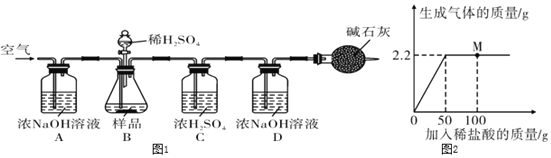
(1)反应结束之后通入空气的目的是_____。
(2)装置A中浓NaOH溶液的作用是_____(用方程式表示)。
(3)实验结束后测得装置D增重0.44g,则湖盐样品中Na2CO3的质量分数为_____%(保留一位小数)。
(4)向6g氯化钠和碳酸钠的固体混合物中不断加入稀盐酸,发生反应的化学方程式为Na2CO3+2HCl═2NaCl+H2O+CO2↑,反应过程中生成气体的质量与加入稀盐酸的质量关系如图2所示。求:
①恰好完全反应时,生成气体的质量为_____。
②M点所对应的溶液中的溶质有_____(填化学式)。
③恰好完全反应时,所得溶液中溶质的质量分数_____。