题目内容
【题目】【改编】(7分)化学实验室要从含有少量铜粉的银、锰(![]() )混合金属粉末中分离出贵金属,并获得一种盐晶体,将有关三种金属随意编号为:A、B、C,并设计了如下流程:
)混合金属粉末中分离出贵金属,并获得一种盐晶体,将有关三种金属随意编号为:A、B、C,并设计了如下流程:
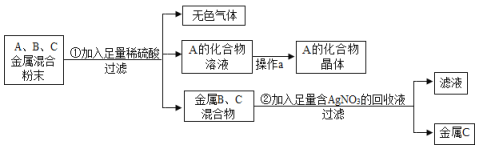
请回答:
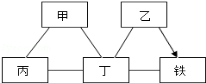
(1)金属C是 ,A、B、C三种金属的活动性顺序为 。
(2)已知A的化合物中A元素显+2价,写出步骤①中反应的化学方程式: (2分);写出步骤②中反应的化学方程式: 。
(3)操作a是 ;有同学觉得过于复杂, (能或者不能)只加入足量AgNO3溶液。
【答案】(1)Ag ; A >B >C ;
(2)![]() ;Cu + 2AgNO3 = 2Ag+ Cu (NO3) 2
;Cu + 2AgNO3 = 2Ag+ Cu (NO3) 2
(3)蒸发结晶 能
【解析】
试题分析:向含有含有少量铜粉的银、锰(![]() )混合金属粉末中加入足量的稀硫酸,锰和稀盐酸反应生成氯化锰和氢气,则A是氯化锰,而铜和银排在氢之后和稀盐酸不反应;向银和铜的混合物中加入足量的硝酸银,铜和硝酸银反应生成硝酸铜和银,硝酸银足量,故铜完全反应,则金属C是银。(1)略;(2)略;(3)将溶于溶液中物质析出,可以蒸发结晶;Mn和Cu的活动性都比Ag更强,都可以与AgNO3置换出Ag,那么只用AgNO3就可以让金属全变为Ag。
)混合金属粉末中加入足量的稀硫酸,锰和稀盐酸反应生成氯化锰和氢气,则A是氯化锰,而铜和银排在氢之后和稀盐酸不反应;向银和铜的混合物中加入足量的硝酸银,铜和硝酸银反应生成硝酸铜和银,硝酸银足量,故铜完全反应,则金属C是银。(1)略;(2)略;(3)将溶于溶液中物质析出,可以蒸发结晶;Mn和Cu的活动性都比Ag更强,都可以与AgNO3置换出Ag,那么只用AgNO3就可以让金属全变为Ag。

练习册系列答案
相关题目