题目内容
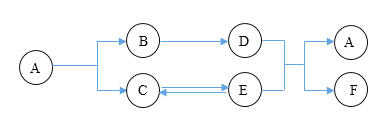
【题目】有一包固体粉末样品M,可能含氧化铜、氧化铝、钢、铝、碳中的一种或几种。为探究样品M的组成,某化学兴趣小组进行了如下图所示实验(部分生成物已省略)。
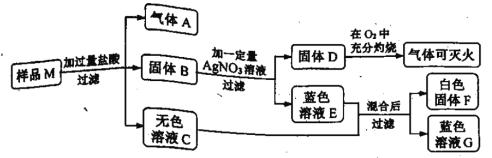
(1)气体是_____。
(2)向固体B中加入硝酸银溶液,发生反应的化学方程式为_____。
(3)样品M中可确定的物质为_____(填化学式,下同)。
(4)蓝色溶液G中一定含有大量的阴离子为_____。
【答案】氢气 ![]() C、CuO、Al
C、CuO、Al ![]()
【解析】
(1)向样品中加入过量稀盐酸产生的气体是氢气。
(2)铜和硝酸银反应生成银和硝酸铜,化学方程式为Cu+2AgNO3==2Ag+Cu(NO3)2。故填:Cu+2AgNO3==2Ag+Cu(NO3)2
(3)样品中加入过量的盐酸,有气体产生,说明样品中一定有铝;固液混合物过滤后,固体B中加入硝酸银溶液,生成蓝色溶液E,铜和硝酸银反应生成银和硝酸铜,得到固体D,D在氧气中灼烧生成二氧化碳,说明固体B中一定有铜、碳,D中一定有碳和银;因此原固体样品中一定含有的物质是碳、氧化铜和铝,化学式为:C、CuO、Al。故填:C、CuO、Al;
(4)蓝色溶液丙中一定含有的溶质是硝酸铝、硝酸铜和硝酸,因为盐酸和硝酸银反应生成氯化银白色沉淀和硝酸。由于反应不知道盐酸和硝酸银哪个有剩余,故氯离子不一定有,所以:大量存在的阴离子是:NO3-;故填:NO3-。

练习册系列答案
相关题目