题目内容
【题目】小明家的“苏打粉”标示的主要成分为碳酸钠和氯化钠。为了测定其中碳酸钠的质量分数,小明取一定量的苏打粉样品于烧杯中并加入质量分数为12%的稀盐酸,当气泡完全放出后,称得反应后烧杯内溶液的质量如图所示。计算:
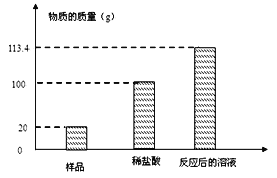
(1)生成的二氧化碳的质量为 .
(2)苏打粉中碳酸钠的质量分数为多少?
【答案】(1)6.6g;(2)79.5%
【解析】(1)根据质量守恒定律,生成二氧化碳的质量是:20g+100g-113.4g=6.6g。
(2)设苏打粉中碳酸钠的质量为x。
Na2CO3 + 2HCl == 2NaCl + H2O + CO2↑
106 44
x 6.6g
![]() =
=![]() ,解得x=15.9g
,解得x=15.9g
苏打粉中碳酸钠的质量分数为: ![]() ×100%=79.5%
×100%=79.5%

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目