题目内容
(2011?呼伦贝尔)根据金属活动性顺序分析,下列描述或判断正确的是( )
分析:A、钾的活动性大于锌的,但应考虑钾的金属活动性太强,它与水反应生成氢氧化钾和氢气;
B、金属铁与硫酸溶液反应生成硫酸亚铁和氢气;
C、根据金属活动性顺序“K、Ca、Na、Mg、Al、Zn、Fe、Sn、Pb、(H)、Cu、Hg、Ag、Pt、Au”可知,金属活动性:Mg>Al;
D、氯化银不溶于水,所以金属铜与氯化银反应不能得到金属银.
B、金属铁与硫酸溶液反应生成硫酸亚铁和氢气;
C、根据金属活动性顺序“K、Ca、Na、Mg、Al、Zn、Fe、Sn、Pb、(H)、Cu、Hg、Ag、Pt、Au”可知,金属活动性:Mg>Al;
D、氯化银不溶于水,所以金属铜与氯化银反应不能得到金属银.
解答:解:A、钾与水反应生成氢氧化钾与硫酸锌反应生成氢氧化锌沉淀和硫酸钾,而不会生成金属锌,故A错误;
B、利用假设法,假设由56克铁与硫酸反应,则生成2克氢气;根据质量守恒定律,则溶液的质量增加了54克,故“金属铁与硫酸溶液反应后所得溶液的质量比原溶液的质量增大”说法正确,故B正确;
C、在常温下,铝比镁更容易与氧气发生化学反应,说法错误,因为金属活动性:Mg>Al,故C错误;
D、因为较活泼的金属能把比它活动性差的金属从它对应的盐溶液中置换出来,而氯化银不溶于水,所以“金属铜与氯化银反应得到金属银”,说法错误,故D错误.
故选B.
B、利用假设法,假设由56克铁与硫酸反应,则生成2克氢气;根据质量守恒定律,则溶液的质量增加了54克,故“金属铁与硫酸溶液反应后所得溶液的质量比原溶液的质量增大”说法正确,故B正确;
C、在常温下,铝比镁更容易与氧气发生化学反应,说法错误,因为金属活动性:Mg>Al,故C错误;
D、因为较活泼的金属能把比它活动性差的金属从它对应的盐溶液中置换出来,而氯化银不溶于水,所以“金属铜与氯化银反应得到金属银”,说法错误,故D错误.
故选B.
点评:熟记金属活动性顺序“K、Ca、Na、Mg、Al、Zn、Fe、Sn、Pb、(H)、Cu、Hg、Ag、Pt、Au”及其应用原则,学会处理实际问题.

练习册系列答案
 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案
相关题目
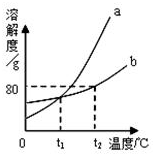 (2011?呼伦贝尔)右图是a、b两种固体物质的溶解度曲线.下列说法正确的是( )
(2011?呼伦贝尔)右图是a、b两种固体物质的溶解度曲线.下列说法正确的是( ) (2011?呼伦贝尔)2010年全国“两会”代表和委员们首次使用环保“石头纸”制作的便笺和文件袋.“石头纸”是一种低碳经济的绿色产品,它的主要成分是一种难溶性钙盐.某化学兴趣小组的同学对“石头纸”的成分进行如右图所示的实验探究,观察到澄清石灰水变浑浊.请回答下列问题:
(2011?呼伦贝尔)2010年全国“两会”代表和委员们首次使用环保“石头纸”制作的便笺和文件袋.“石头纸”是一种低碳经济的绿色产品,它的主要成分是一种难溶性钙盐.某化学兴趣小组的同学对“石头纸”的成分进行如右图所示的实验探究,观察到澄清石灰水变浑浊.请回答下列问题: