题目内容
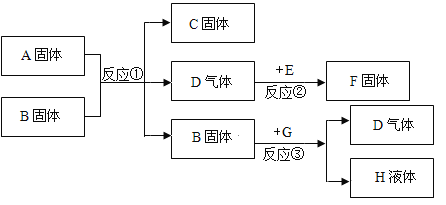
【题目】氧化铜有多种用途,如用作玻璃着色剂、油类脱油剂等。为获得纯净的氧化铜以探究其性质,某同学用工业硫酸铜(含杂质)进行如下实验:
![]()
(1)制备氧化铜
①步骤Ⅰ的目的是除不溶性杂质,操作是__________。
②步骤ⅡⅠ的目的是得到CuSO4·5H2O晶体。操作顺序是b→________→_________→d。
a过滤 b加热浓缩 c冷却结晶 d洗涤干燥
③在CuSO4·5H2O晶体最终转变为纯净CuO的过程中,观察到蓝色晶体先变为______色,最终变为________色。
(2)探究氧化铜的性质
①取A、B两支试管,往A中先加适量CuO粉末,再分别向A、B中加入等体积的3% H2O2溶液,只观察到A中有大量气泡,该气体能使带火星的木条复燃。则CuO的作用是________。反应的化学方程式为____________。
②取3.2g CuO粉末,隔绝空气加强热,除产生一种无色气体外,还残留2.88g砖红色固体,则其化学式为___________。
【答案】过滤 c a 白 黑 CuO可加快双氧水分解的速度(催化作用) 2H2O2![]() 2H2O + O2↑ Cu2O
2H2O + O2↑ Cu2O
【解析】
(1)①步骤I的目的是除去不溶性杂质,操作是过滤。
故填:过滤.
②步骤Ⅱ的目的是得到CuSO45H2O晶体,操作顺序是:加热浓缩→冷却结晶→过滤→洗涤干燥.
故填:c;a.
③将CuSO45H2O晶体加热最终获得纯净CuO的过程中,五水硫酸铜先失去结晶水,后硫酸铜分解生成氧化铜,能够观察到蓝色晶体先变为白色,最终变为黑色.
故填:白;黑.
(2)①取A、B两支试管,往A中先加入适量CuO粉末,再分别向A 和B中加入等体积的3%H2O2溶液,只观察到A中有大量气泡,该气体能使带火星木条复燃,说明CuO可加快H2O2分解的反应速率,是H2O2分解反应的催化剂,反应方程式为:2H2O2![]() O2↑+2H2O.
O2↑+2H2O.
故填:CuO可加快H2O2分解的反应速率,是H2O2分解反应的催化剂;2H2O2![]() O2↑+2H2O.
O2↑+2H2O.
②3.2gCuO中含有氧元素质量为:3.2g×![]() ×100%=0.64g,铜元素质量为:3.2g-0.64g=2.56g,粉末隔绝空气加强热,除产生氧气外,还残留2.88g砖红色固体,则2.88g固体中含有铜元素的质量是2.56g,含有氧元素质量为:2.88g-2.56g=0.32g,
×100%=0.64g,铜元素质量为:3.2g-0.64g=2.56g,粉末隔绝空气加强热,除产生氧气外,还残留2.88g砖红色固体,则2.88g固体中含有铜元素的质量是2.56g,含有氧元素质量为:2.88g-2.56g=0.32g,
设铜元素和氧元素组成的化合物中原子个数比是x:y,则有64x:16y=2.56g:0.32g,
x:y=2:1,则其化学式为Cu2O。
故填:Cu2O.

【题目】某学习小组的同学前往当地的石灰石矿区进行调查,他们取了若干块矿石样品,对样品中的碳酸钙的质量分数进行检测,采用了以下的办法:取用12. 0g这种石灰石样品,把40.0g稀盐酸分四次加入,测量过程所得数据见下表(杂质不溶于水,不与盐酸反应)。
序号 | 第一次 | 第二次 | 第三次 | 第四次 |
加入稀盐酸质量(g) | 10.0 | 10.0 | 10.0 | 10.0 |
剩余固体质量(g) | 8.0 | m | 2.0 | 2.0 |
请计算: (1) 表中的m的数值应为_____;
(2)样品中的碳酸钙的质量分数是_____;
(3)产生二氧化碳的总质量是多少?_____
【题目】实验是科学探究的重要方法。如图是测定空气中氧气含量实验的两套装置图,请结合图示回答有关问题。已知:铜+氧气→氧化铜(黑色固体)
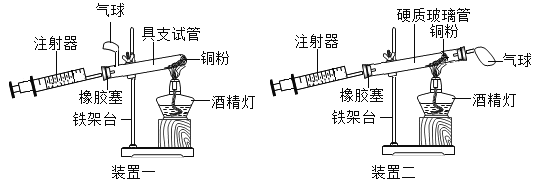
(1) 根据下表提供的实验数据,完成下表
硬质玻璃管中空气的体积 | 反应前注射器中空气体积 | 反应后注射器中气体体积 | 实验测得空气中氧气的体积分数 |
25mL | 15mL | 9mL | _________________。 |
(2)装置一和装置二中气球的位置不同,_________________装置 (填“一”或“二”)更合理。