题目内容
【题目】工业上利用某废渣(含FeSO4、Fe2(SO4)3及少量CaO和MgO)制备高档颜料铁红(主要成分为Fe2O3)和回收(NH4)2SO4,其生产流程如下:
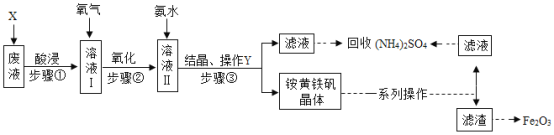
已知:a、氧化还原反应中,会有元素化合价发生变化。
b、![]() 回答下列问题:
回答下列问题:
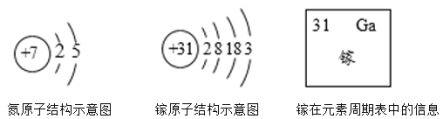
(1)(NH4)2Fe6(SO4)4(OH)12中铁元素的化合价是_____。
(2)粉碎废渣的目的_____,加入物质X溶解废渣,X应选用_____(填序号)。
A 盐酸
B 硫酸
C 氨水
D 氢氧化钠
步骤①酸浸时,生成盐的化学方程式为_____(任写一个)。
(3)步骤③中操作Y的名称是____,滤液中除含有很少量铵黄铁矾外还含有__。
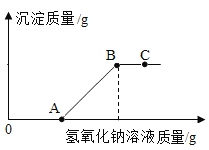
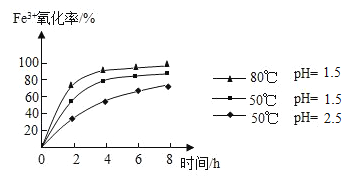
(4)步骤②通入氧气氧化的目的是_____,工业上对该操作控制在4小时左右为宜,根据如图有关数据分析,影响Fe3+氧化率的变化规律:_____。
【答案】+3 增大反应物之间的接触面积,使反应充分进行 B ![]() (或
(或![]() ) 过滤 硫酸钙、硫酸镁、硫酸铵[或CaSO4、MgSO4、(NH4)2SO4] 将亚铁离子(或Fe2+)氧化成三价铁离子(或Fe3+) 温度越高,pH越小(或酸性越强),三价铁离子(或Fe2+)氧化率越高
) 过滤 硫酸钙、硫酸镁、硫酸铵[或CaSO4、MgSO4、(NH4)2SO4] 将亚铁离子(或Fe2+)氧化成三价铁离子(或Fe3+) 温度越高,pH越小(或酸性越强),三价铁离子(或Fe2+)氧化率越高
【解析】
氧化镁和硫酸生成硫酸镁和水,氧化钙和硫酸生成硫酸钙和水,粉碎废渣的目的增大反应物之间的接触面积,使反应充分进行。
(1)(NH4)2Fe6(SO4)4(OH)12中铵根离子的化合价为+1价,硫酸根离子的化合价为-2价,氢氧根离子的化合价为-1价,设铁元素的化合价是x,化合物中各元素的正负化合价代数和为零,则![]() ,
,![]() ,故铁元素的化合价是+3价。
,故铁元素的化合价是+3价。
(2)粉碎废渣的目的增大反应物之间的接触面积,使反应充分进行,废渣中含有氧化钙和氧化镁,氧化镁和硫酸生成硫酸镁和水,氧化钙和硫酸生成硫酸钙和水,加入物质X溶解废渣,X应选用硫酸,故选B。
步骤①酸浸时,生成盐的反应是氧化镁和硫酸生成硫酸镁和水,或氧化钙和硫酸生成硫酸钙和水,故反应的化学方程式为![]() (或
(或![]() )。
)。
(3)步骤③中操作Y是将固体和液体分离,故名称是过滤,氧化镁和硫酸生成硫酸镁,氧化钙和硫酸生成硫酸钙,氨水和硫酸铁生成硫酸铵,故滤液中除含有很少量铵黄铁矾外还含有硫酸钙、硫酸镁、硫酸铵[或CaSO4、MgSO4、(NH4)2SO4]。
(4)生产流程需要将硫酸亚铁氧化成硫酸铁和氨水反应,故步骤②通入氧气氧化的目的是将亚铁离子(或Fe2+)氧化成三价铁离子(或Fe3+),由图像可知,铁离子的氧化率随着酸性的减弱而减小,故工业上对该操作控制在4小时左右为宜,根据如图有关数据分析,影响Fe3+氧化率的变化规律是温度越高,pH越小(或酸性越强),三价铁离子(或Fe2+)氧化率越高。