��Ŀ����
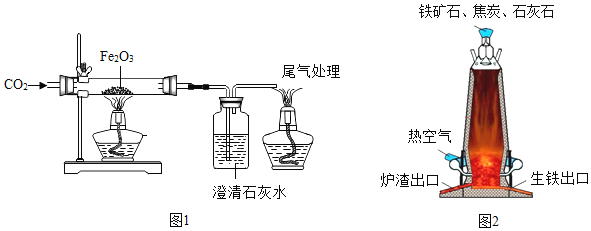
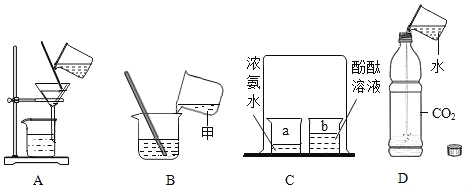
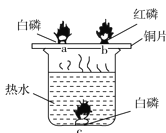
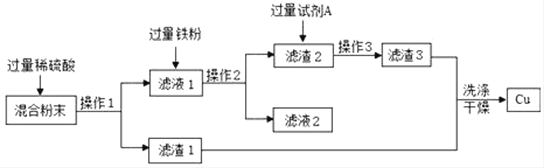
����Ŀ����ѧ��ȤС��ͬѧ������ľ̿�ۻ�ԭ����ͭʵ���Ļ�Ϸ�ĩ�����к���ͭ������ͭ������ľ̿�ۣ� ����ͭ��ʵ�����������ͼ��ʾ��
��ش��������⣺
��1���ڲ��� 1������ 2������ 3 �У������õ��IJ��������У��ձ�����������_____�����в�������������_____��
��2����Һ 1 �м�����������������Ļ�ѧ����ʽ��_____�������Լ� A ��������_____��
��3������ʵ�����̲������յ��� Cu ������ԭ����_____��
���𰸡�©���� ���� Fe+CuSO4��FeSO4+Cu��Fe+H2SO4��FeSO4+H2�� ��ȥ���������ۣ��ᴿͭ ���� 1 �к���ľ̿��
��������
����ͼ��Ϸ�ĩ�к���ͭ������ͭ������ľ̿�ۣ����������ϡ���ᣬ����ͭ��ϡ���ᷴӦ��������ͭ����Һ1����Ҫ������ͭ���������ᣬ������������۰�ͭ�û��������������ˣ���ͭ�����Ļ�����˳�������2�У���֪������2�м����Լ�A������ȥ���������1����õ�ͭ��
I.��������ͼ������֪������������Ϊ���ˣ���Ҫ�IJ��������У��ձ��������塢©�������ڲ��� 1������ 2������ 3 �У������õ��IJ��������У��ձ�����������©���� ���в����������������������©��������
II.��Һ 1 ����Ҫ�ɷ�������ͭ�����ᣬ������������������Ļ�ѧ����ʽ���������ֱ���Fe+CuSO4��FeSO4+Cu��Fe+H2SO4��FeSO4+H2������Ϊ����2�л����������������ʣ�Ҫ�õ�ͭ�����������ȥ���ʼ����Լ� A �������dz�ȥ���������ۣ��ᴿͭ�����Fe+CuSO4��FeSO4+Cu��Fe+H2SO4��FeSO4+H2�� ����ȥ���������ۣ��ᴿͭ
III.������ͼ��֪����������к���������̼�ۣ�����������֮�������ᷴӦ��Ҳ������ˮ���ʴ�������1�У�ʹ��ͭ�����л���������̼�ۣ��ʰ���ʵ�����̲������յ��� Cu ������ԭ�������� 1 �к���ľ̿�ۡ�������� 1 �к���ľ̿��

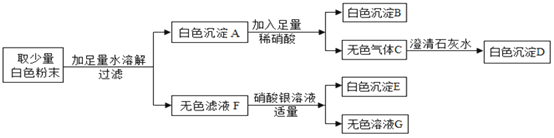
����Ŀ��A��B��C��D��E��F �� H2��CuO��Na2CO3��HCl��Ca(OH)2��CO2 �е�һ�֣��Ѳ��� ����������Ͻ���ʵ�飬�������±���
������� | B+C | C+D | D+E |
���� | �������� | �������� | �������� |
��1��B �� C ���ʱ������������_____��д��ѧʽ����ͬ����D ������_____��
��2��A + F �Ļ�ѧ����ʽ��_____��
��3��������������֮���ܷ����ĸ��ֽⷴӦһ����_____����
��4���������������У��е�����֮����˫��ת������__________���ѧʽ����