题目内容
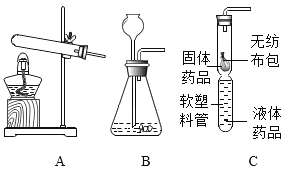
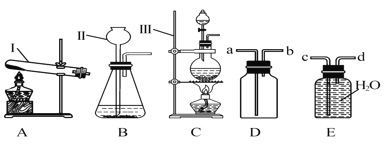
【题目】根据下图回答问题:
资料:①制取Cl2: MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
②Cl2是一种黄绿色、有刺激性气味、密度比空气大、能溶于水的气体。
(1)仪器Ⅱ的名称_____
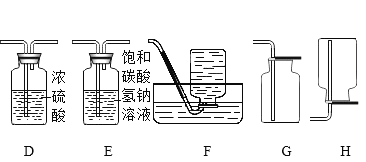
(2)写出实验室制取CO2的化学方程式____。用D装置干燥二氧化碳,则D中应装入___,此干燥剂不能干燥的气体_(填化学式)
(3)用C装置制取氯气原因:一是反应需要加热、二是_____。用D装置收集Cl2时,Cl2应从__(填导气管接口处的字母)管口进入瓶中。
(4)用氯酸钾制取氧气方程式_____,反应后从剩余固体中分离出MnO2的实验步骤有溶解、过滤和洗涤。过滤时玻璃棒的作用是____。
(5)下列对制取三种气体的分析中不正确的是_。
A 制取CO2和O2可以用相同的发生装置
B O2、CO2和Cl2都能用向上排空气法收集
C 制取Cl2的反应中MnO2是催化剂
D 用E装置收集O2时,O2应从d管导入
【答案】长颈漏斗 CaCO3 + 2HCl = CaCl2 + H2O + CO2↑ 浓硫酸 NH3 反应物状态有液体 a 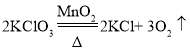 引流 C
引流 C
【解析】
(1)由图可知仪器Ⅱ为长颈漏斗,故填:长颈漏斗。
(2)实验室用石灰石或大理石和稀盐酸反应制取二氧化碳,化学方程式为CaCO3 + 2HCl = CaCl2 + H2O + CO2↑,浓硫酸具有吸水性,D装置干燥二氧化碳,则D中应装入浓硫酸,浓硫酸能和氨气反应,不能干燥氨气,故填:CaCO3 + 2HCl = CaCl2 + H2O + CO2↑;浓硫酸; NH3。
(3)用C装置制取氯气原因:一是反应需要加热、二是反应物状态有液体,用D装置收集Cl2时因为氯气密度比空气大,Cl2应从a管口进入瓶中,故填:反应物状态有液体;a。
(4)氯酸钾加热生成氯化钾和氧气,化学方程式为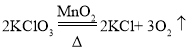 ,反应后从剩余固体中分离出MnO2的实验步骤有溶解、过滤和洗涤。过滤时玻璃棒的作用是引流,故填:
,反应后从剩余固体中分离出MnO2的实验步骤有溶解、过滤和洗涤。过滤时玻璃棒的作用是引流,故填: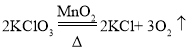 ;引流。
;引流。
(5)A、 制取CO2和O2都可以用固液不加热的反应装置,故A正确。
B、O2、CO2和Cl2密度都比空气大,都能用向上排空气法收集,故B正确。
C、制取Cl2的反应中MnO2是反应物,不是催化剂,C错。
D、 用E装置收集O2时因为氧气密度比水小且氧气不易溶于水,故O2应从d管导入,D正确。
故选:C。

【题目】2020年我国在部分地区和领域禁塑限塑。化学杜团同学对平常在超市买东西时带回来的塑料袋进行探究。
[查阅资料]日常生活中使用的塑料袋有用聚乙烯制成的,也有用聚氯乙烯制成的。聚乙烯燃烧生成CO2和H2O;聚氯乙烯燃烧除了生成CO2和H2O之外,还会有HCl气体产生;无水氯化钙可用作干燥剂。
探究一、该塑料袋的材料是什么
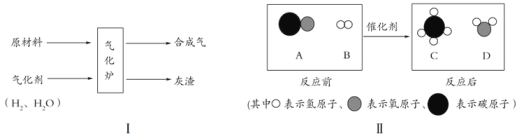
[实验]小明将该塑料袋样品在氧气中燃烧的产物通入下图一的装置进行探究。
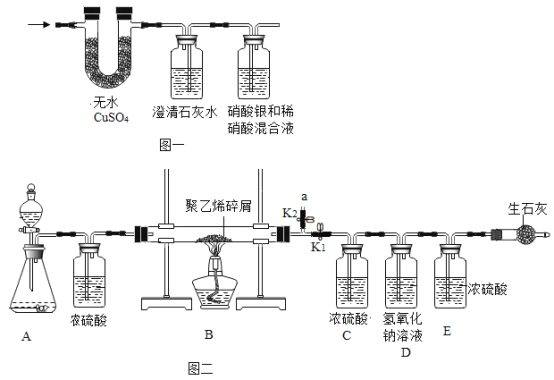
[质疑]李蕾认为小明设计的装置无法得出正确的结论,他的依据是______________。经完善装置,确认该塑料袋的材料是聚乙烯。
探究二、探究聚乙烯的组成碎屑
[实验设计]小组同学设计上图二所示装置。
[分析] A装置是氧气发生装置,反应原理为________________(用化学方程式表示)。
[实验操作]称取5.6g样品碎屑于B处硬质玻璃管中,排出装置中空气后,通入足量的氧气使样品充分燃烧,并将产生的气体通入足量的浓硫酸和氢氧化钠溶液中。
[数据记录]实验结果:
样品燃烧前 | 样品燃烧后 | |
C装置的质量/g | 213.6 | 220.8 |
D. E装置的总质量/g | 440.2 | 457.8 |
[分析与结论]聚乙烯中____________(填“含”或“不含”氧元素,聚乙烯中碳元素,氢元素的质量比为______。
[反思]如果没有E装置,对所测碳元素的质量的影响是___ (填 “偏大”“无影响”或“偏小”)。