题目内容
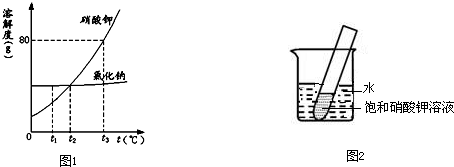
图1是氯化钠和硝酸钾两种物质的溶解度曲线,图2是氢氧化钙的溶解度曲线.根据图示回答下列问题.
(1)硝酸钾溶液中的溶质为 .10℃时氯化钠的溶解度 (填“大于”“小于”或“等于”)硝酸钾的溶解度.将30℃时的硝酸钾饱和溶液转变为不饱和溶液的一种方法是 .从氯化钠溶液中结晶出氯化钠的方法是 .
(2)某同学从一瓶久置于空气中的氢氧化钙固体样品(标签为纯净物)中取出0.2g,加入到30℃时100g水中,充分溶解后过滤,称得剩余固体0.08g.请你判断:
滤液为 (填“饱和”或“不饱和”)溶液,剩余固体的成分为 .
(3)将20℃时恰好饱和的硝酸钾溶液升温至60℃,一定没有变化的是 (填序号).
①水的质量 ②溶液中溶质的质量 ③硝酸钾的溶解度.
【答案】分析:(1)运用硝酸钾溶于水形成硝酸钾溶液、题中溶解度曲线图某一点的意义、硝酸钾的溶解度随温度升高而增大、氯化钠的溶解度受温度影响不大冷却热饱和溶液不会结晶形成或析出很少只能运用蒸发溶剂的方法结晶解答.
(2)运用30℃时氢氧化钙的溶解度为0.15g,也就是说该温度下100g溶剂水中达到饱和状态所溶解的溶质氢氧化钙的质量是0.15g和氢氧化钙和二氧化碳反应生成碳酸钙沉淀和水解答.
(3)运用温度升高硝酸钾的溶解度增大,溶液由饱和变为不饱和但溶质和溶剂的质量都不变解答.
解答:解:(1)硝酸钾溶于水形成硝酸钾溶液,所以硝酸钾溶液中的溶质是硝酸钾;从溶解度曲线可看出10℃时氯化钠的溶解度大于硝酸钾的溶解度;硝酸钾的溶解度随温度升高而增大,所以升高温度硝酸钾的饱和溶液变为不饱和溶液,加溶剂所有的饱和溶液都会变为不饱和溶液;氯化钠的溶解度受温度影响不大冷却热饱和溶液不会结晶形成或析出很少只能运用蒸发溶剂的方法结晶;故答案:(1)KNO3;大于;加水或升温;蒸发溶剂.
(2)30℃时氢氧化钙的溶解度为0.15g,即该温度下100g溶剂水中达到饱和状态所溶解的溶质氢氧化钙的质量是0.15g,由题意知该温度下100g水中溶解了0.12g,所以所得溶液不饱和.如果全是氢氧化钙剩余的不溶固体应该是0.05g,剩余固体0.08g所以可以肯定一部分氢氧化钙已经和二氧化碳反应,氢氧化钙和二氧化碳反应生成碳酸钙沉淀和水,所以久置于空气中的氢氧化钙固体样品中含有碳酸钙.故(2)答案:不饱和;碳酸钙.
(3)温度升高硝酸钾的溶解度增大,溶液由饱和变为不饱和,溶质不会析出溶剂也不蒸发所以溶质和溶剂的质量都不变,故(3)答案:①②.
点评:溶解度曲线能定量地表示出溶解度变化的规律,从溶解度曲线可以看出:同一溶质在不同温度下的溶解度;同一温度下,不同溶质的溶解度;温度对不同物质的溶解度影响不同,要注意固体的溶解度是一定温度下100g溶剂水达到饱和状态所溶解的溶质的质量,要抓住关键四个因素:一定温度 100g溶剂 饱和状态 溶解的溶质质量.
(2)运用30℃时氢氧化钙的溶解度为0.15g,也就是说该温度下100g溶剂水中达到饱和状态所溶解的溶质氢氧化钙的质量是0.15g和氢氧化钙和二氧化碳反应生成碳酸钙沉淀和水解答.
(3)运用温度升高硝酸钾的溶解度增大,溶液由饱和变为不饱和但溶质和溶剂的质量都不变解答.
解答:解:(1)硝酸钾溶于水形成硝酸钾溶液,所以硝酸钾溶液中的溶质是硝酸钾;从溶解度曲线可看出10℃时氯化钠的溶解度大于硝酸钾的溶解度;硝酸钾的溶解度随温度升高而增大,所以升高温度硝酸钾的饱和溶液变为不饱和溶液,加溶剂所有的饱和溶液都会变为不饱和溶液;氯化钠的溶解度受温度影响不大冷却热饱和溶液不会结晶形成或析出很少只能运用蒸发溶剂的方法结晶;故答案:(1)KNO3;大于;加水或升温;蒸发溶剂.
(2)30℃时氢氧化钙的溶解度为0.15g,即该温度下100g溶剂水中达到饱和状态所溶解的溶质氢氧化钙的质量是0.15g,由题意知该温度下100g水中溶解了0.12g,所以所得溶液不饱和.如果全是氢氧化钙剩余的不溶固体应该是0.05g,剩余固体0.08g所以可以肯定一部分氢氧化钙已经和二氧化碳反应,氢氧化钙和二氧化碳反应生成碳酸钙沉淀和水,所以久置于空气中的氢氧化钙固体样品中含有碳酸钙.故(2)答案:不饱和;碳酸钙.
(3)温度升高硝酸钾的溶解度增大,溶液由饱和变为不饱和,溶质不会析出溶剂也不蒸发所以溶质和溶剂的质量都不变,故(3)答案:①②.
点评:溶解度曲线能定量地表示出溶解度变化的规律,从溶解度曲线可以看出:同一溶质在不同温度下的溶解度;同一温度下,不同溶质的溶解度;温度对不同物质的溶解度影响不同,要注意固体的溶解度是一定温度下100g溶剂水达到饱和状态所溶解的溶质的质量,要抓住关键四个因素:一定温度 100g溶剂 饱和状态 溶解的溶质质量.

练习册系列答案
相关题目