��Ŀ����
����Ŀ����������װ��ͼ���ش����⣺
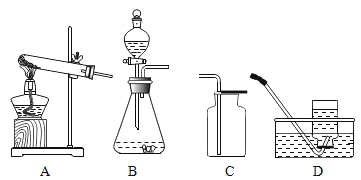
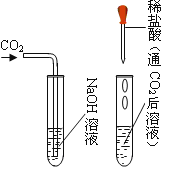
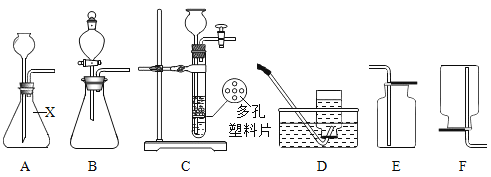
��1�����������ȡ������ѡ�õķ���װ����______������ţ���Ӧ�Ļ�ѧ����ʽΪ______������Dװ���ռ����������۲쵽______ʱ����ɿ�ʼ�ռ���
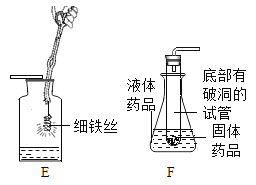
��2��ʵ������ȡ������̼��Ӧ�Ļ�ѧ����ʽ��______��ͼF�����ñ����Թ���Ƶ���ȡ������̼�ķ���װ�ã�����Ƴ��˷������õ��ŵ��⣬����дһ���ŵ�______��
��3�����ռ����������ͼE��˿ȼ�յ�ʵ�鼯��ƿ��Ԥ�ȷ�����ˮ��ԭ����______��
���𰸡�A 2KClO3![]() 2KCl+3O2�� ��������ð�� CaCO3+2HCl�TCaCl2+H2O+CO2�� ��ʹ��Ӧ��ʱ���л�ֹͣ �ܹ���ֹ��ȼ���γɵĸ��������ヲ��ը�Ѽ���ƿ
2KCl+3O2�� ��������ð�� CaCO3+2HCl�TCaCl2+H2O+CO2�� ��ʹ��Ӧ��ʱ���л�ֹͣ �ܹ���ֹ��ȼ���γɵĸ��������ヲ��ը�Ѽ���ƿ
��������
��1�����������ȡ������Ҫ���ȣ�Ӧѡ�ü��ȹ�����ȡ����װ�ã�ѡ�õķ���װ����A����Ӧ�Ļ�ѧ����ʽΪ��2KClO3![]() 2KCl+3O2����Ϊ�ռ��������������壬����Dװ���ռ����������۲쵽��������ð��ʱ����ʼ�ռ���
2KCl+3O2����Ϊ�ռ��������������壬����Dװ���ռ����������۲쵽��������ð��ʱ����ʼ�ռ���
��2��ʵ�����ô���ʯ��ʯ��ʯ��ϡ������ȡ������̼����ȡ������̼��Ӧ�Ļ�ѧ����ʽ�ǣ�CaCO3+2HCl�TCaCl2+H2O+CO2����ͼF��Ƴ��˷������õ��ŵ��⣬��һ���ŵ�����ʹ��Ӧ��ʱ���л�ֹͣ��
��3�����ռ����������ͼE��˿ȼ�յ�ʵ�鼯��ƿ��Ԥ�ȷ�����ˮ��ԭ���Ƿ�ֹ��ȼ���γɵĸ��������ヲ��ը�Ѽ���ƿ��

����Ŀ��ij��ѧʵ��С����̽��CO2��NaOH�Ƿ�����Ӧʱ��С����Ƴ���������װ�ý���ʵ�飺
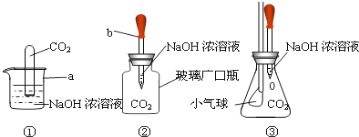
��ش����¼������⣺
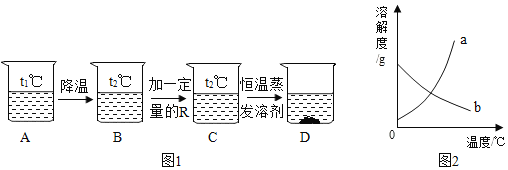
��1��д����ͼ�б�����ĸ���������ƣ�a___________��
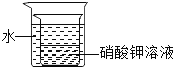
��2����������ʵ���У��٢����������������С����¼���۲쵽��ʵ������ʵ���_________��ʵ���_________��
��3��ʵ�����ѡ��������������δ�ܹ۲쵽�������������С��Ѱ��һ����Ʒ�����װ���еĹ��ƿ����ʹʵ��ȡ�óɹ����㽫ѡ�õ���Ʒ��_________���Ľ����ܿ�����ʵ��������____________��
��4��С��ͬѧ��������ɣ�����ΪС��ʵ�黹������֤��CO2��NaOHȷʵ�����˷�Ӧ����������___________��
��5��С��ͬѧ�ֲ��䡢�������ʵ�鷽������һ��֤��������������ɣ�
ʵ�鲽��ͷ��� | ʵ������ | ʵ����ۣ��÷���ʽ��ʾ�� |
| ___________ | д����ͼ���漰��������Ӧ�Ļ�ѧ����ʽ___________��_______�� |
����Ŀ����ʦ�ڷ�������������Һ��Ӧʱָ���ڽ�����Ե�˳����,λ��ǰ��Ľ����ܰ����ں���Ľ��������ǵ�����Һ���û����������ء��ơ��Ƴ��⡣����ͬѧ�ܺ���,����������������ͭ��Һ��Ӧ��ʵ�顣
���������飩
һ��4.6g�Ľ����ƣ�����ʢ��һ��������ͭ��Һ���ձ���,���ֽ����Ƹ���Һ���ϲ�ͣ��ת��������������,�ձ����̣���Һ�г�������ɫ��״����,��û�г����Ϻ�ɫ��ͭ��һ��������ֳ�����ڡ���ַ�Ӧ��,��ȴ���ˣ��õ���Һ����ɫ��
��������⣩
������������ͭ��Һ��Ӧ��IJ�����ʲô?��ɫ��Һ�ijɷ���ʲô?
���������ϣ�
(1)��������ˮ��Ӧ����һ�ּͬʱ�ų����塣
��������ͭ������60�� ~80��䰵,�¶ȹ���ʱ�ֽ�Ϊ��Ӧ�Ľ����������ˮ��
��ʵ��̽��1��̽�����ɵ�������ʲô?
����ͬѧ������ʵ��ҩƷ������ƿ�У��������ϴ����ܵĵ�����,������ͨ�����ˮ�У���ȼ�ŵ�ľ������Ʈ��ķ����ݣ��б�������˵�����ɵ�������____________��
��ʵ��̽��2��̽�������ijɷ���ʲô?
����������裩��������Cu(OH)2��CuO�������ܺ���Cu��
��ʵ����֤��
ʵ�鲽�� | ʵ������ | ���� |
����ƿ�ڷ�Ӧ������������������ձ��ڣ�������������______ | _________ | ������û��Cu |
��ʵ����ۣ�
ͨ��ʵ��,����ͬѧ�ó�����:�Ƽ�������ͭ��Һ������ˮ��Ӧ,���ɵļ���������ͭ��Ӧ����������ͭ��д�����ɵļ�������ͭ��Ӧ�Ļ�ѧ����ʽ______________��
��ʵ��̽��3����Һ�ijɷ���ʲô?
ͨ������,����ͬѧ�ó�:���õ���ɫ��Һ��һ������������,�����ܺ���______________��
��Ҫ֤���Ƿ��и����ʣ�ֻ������ɫ��Һ�еμ�______________ (����������)�۲����ɻ�ý��ۡ�
����˼�뽻����
(1)���ֺ�ɫ���ʵĿ���ԭ����______________��
(2)���һ����ʵ��֤������ͭ��Һ����ɫ����Cu2+����ġ���ķ�����______________��(Ҫ��д��ʵ�鲽�������)
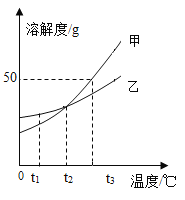
(3)����ȫ���ɺ�������ɫ��Һ�������Ƶ���������a��ʾ����a��ȡֵ��Χ��______________��