题目内容
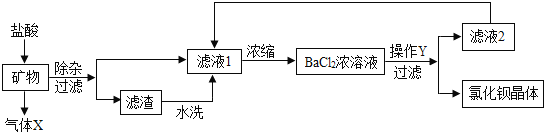
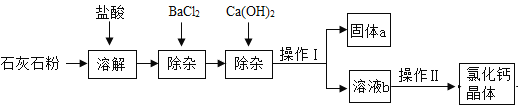
【题目】轻质碳酸钙广泛应用于橡胶、塑料、油漆、水性涂料以及造纸等行业,日常生活中的牙膏也常用它作摩擦剂.此碳酸钙粉末的制备过程为:
①煅烧石灰石(石灰石中的杂质高温不分解且不溶于水);
②加水充分反应后过滤;
③向Ca(OH)2溶液中通入二氧化碳得到碳酸钙.
请分析轻质碳酸钙的制备过程,回答下列问题:
(1)过滤操作中玻璃棒的作用是________.
(2)化工生产要贴合“环境友好,绿色化学”.③中通入的CO2最好来源于________.
(3)由于过量的CO2能与碳酸钙反应,化学方程式为:CaCO3+CO2+H2O=Ca(HCO3)2.在③中通入的CO2不能过量,如果工厂需要10t轻质碳酸钙,需要通入CO2的质量为________t.
(4)生产轻质碳酸钙的方法有很多,如向氢氧化钙溶液中通入CO2,反应的化学方程式为________,也可以向氢氧化钙溶液中加入________溶液.
【答案】引流 煅烧石灰石生成的二氧化碳 4.4 ![]() 碳酸钠
碳酸钠
【解析】
碳酸钙高温生成氧化钙和二氧化碳,二氧化碳和氢氧化钙反应生成碳酸钙和水,氢氧化钙能与碳酸钠反应生成碳酸钙沉淀和氢氧化钠。
(1)过滤中玻璃棒起到的是引流的作用。
(2)碳酸钙高温生成氧化钙和二氧化碳,二氧化碳和氢氧化钙反应生成碳酸钙,故③中通入的CO2最好来源是煅烧石灰石生成的二氧化碳。
(3)需要10t轻质碳酸钙,设需要通入CO2的质量为x

![]()
![]()
故如果工厂需要10t轻质碳酸钙,需要通入CO2的质量为4.4t。
(4)氢氧化钙能与二氧化碳反应生成碳酸钙沉淀和水,反应的化学方程式为![]() ,氢氧化钙能与碳酸钠反应生成碳酸钙沉淀和氢氧化钠,故也可以向氢氧化钙溶液中加入碳酸钠溶液。
,氢氧化钙能与碳酸钠反应生成碳酸钙沉淀和氢氧化钠,故也可以向氢氧化钙溶液中加入碳酸钠溶液。

 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案【题目】下列实验方法不能达到实验目的的是
选项 | 实验目的 | 实验方法 |
A | 除去MnO2固体中的KCl | 加水溶解,过滤,洗涤,干燥 |
B | 鉴别化肥NH4Cl和KNO3 | 取少量化肥加入熟石灰粉末研磨,闻气味 |
C | 配制质量分数为6%的NaCl溶液 | 称取3.0g NaCl,加入50.0mL水使之溶解 |
D | 鉴定本地雨水是否为酸雨 | 用pH计测定雨水的pH |
A. AB. BC. CD. D