题目内容
【题目】(10分)为了测定某样品中氧化铁(Fe2O3)的质量分数(杂质不含铁元素,且不溶于水和酸),化学兴趣小组的同学进行了如下的实验。
【查阅资料】
1.草酸(H2C2O4)在浓硫酸作用下受热分解,化学方程式为:
H2C2O4 ![]() CO2↑+CO↑+H2O
CO2↑+CO↑+H2O
2.碱石灰能吸收二氧化碳和水蒸气
【实验设计及操作】用下图所示装置进行实验:
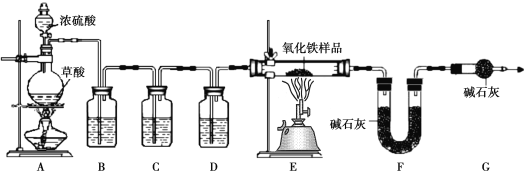
【问题讨论】
(1)装药品前应先,实验中观察到E中现象是:固体颜色 ;
(2)进入E中的气体是纯净、干燥的CO,则B、C、D中依次是(填序号)。
① 浓硫酸、石灰水、氢氧化钠溶液
② 石灰水、氢氧化钠溶液、浓硫酸
③ 氢氧化钠溶液、石灰水、浓硫酸
(3)G的作用是 ;E中反应的化学方程式是 ;
(4)当E中固体完全反应后, 处应先停止加热(填序号A或E);
(5)上述实验装置的一处明显缺陷是: 。
【数据处理】
称取样品8.0g,用上述装置进行实验,充分反应后称量F装置增重4.4g。则样品中氧
化铁质量分数为 。
【实验反思】
当观察到E中固体全部变黑后,若立即停止通CO,则测得的样品中氧化铁的质量分数
(填“偏大”,“偏小”,“无影响”)。
【答案】【问题讨论】(1)检查装置的气密性 由红色变为黑色
(2)③ (3)隔离空气中的二氧化碳和水蒸气 Fe2O3+3CO![]() 2Fe+3CO2
2Fe+3CO2
(4)E (5)未进行尾气处理
【数据处理】66.7% 【数据处理】偏小
【解析】
试题分析:【问题讨论】(1)有气体参加、生成的反应,为了防止漏气,装药品前应先检查装置的气密性,实验中E中发生的反应方程式为:Fe2O3+3CO![]() 2Fe+3CO2,观察到现象是:固体颜色由红色变为黑色
2Fe+3CO2,观察到现象是:固体颜色由红色变为黑色
(2)干燥气体应放在最后一步,氢氧化钠溶液是吸收二氧化碳,而石灰水是检验二氧化碳,所以进入E中的气体是纯净、干燥的CO,则B、C、D中依次是氢氧化钠溶液、石灰水、浓硫酸,选③
(3)G的作用是:隔离空气中的二氧化碳和水蒸气,防止空气中的二氧化碳和水蒸气进入到装置F中,从而使二氧化碳质量偏大,E中反应的化学方程式是:Fe2O3+3CO![]() 2Fe+3CO2
2Fe+3CO2
(4)当E中固体完全反应后,还要继续通入一氧化碳,防止灼热的铁又与空气中的氧气反应,使实验失败,且装置E中产生的二氧化碳还有部分没有进入到装置F中,所以E处应先停止加热
(5)因为一氧化碳有毒,所以上述实验装置的一处明显缺陷是:未进行尾气处理
【数据处理】充分反应后称量F装置增重4.4g,即反应生成的二氧化碳质量为4.4g,再根据反应方程式:Fe2O3+3CO![]() 2Fe+3CO2中Fe2O3与CO2的质量关系,即可求出Fe2O3的质量,进而计算样品中氧化铁质量分数
2Fe+3CO2中Fe2O3与CO2的质量关系,即可求出Fe2O3的质量,进而计算样品中氧化铁质量分数
解:设Fe2O3的质量为x
Fe2O3+3CO![]() 2Fe+3CO2
2Fe+3CO2
160 132
x 4.4g
160:132=x:4.4g
X=5.33g
∴样品中氧化铁质量分数=5.33g/8.0g×100%=66.7%
【数据处理】当观察到E中固体全部变黑后,若立即停止通CO,装置E中产生的二氧化碳还有部分没有进入到装置F中,使二氧化碳的质量偏小,则测得的样品中氧化铁的质量分数也偏小

 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案 英才计划同步课时高效训练系列答案
英才计划同步课时高效训练系列答案