题目内容
【题目】为测定某大理石样品中碳酸钙的质量分数,取该样品10g,加入足量的10%盐酸,产生CO2 的物质的量与时间的关系如图所示(杂质不含碳元素)。
![]()
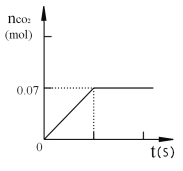
①该样品中碳酸钙的质量分数。(根据化学方程式列式计算)(19)
②若取该样品10g,充分煅烧,最多可以产生CO2 (20) g。
【答案】①70%;② 3.08
【解析】
试题分析:解:设含有xmol CaCO3
CaCO3+2HCl![]() CaCl2+CO2↑+H2O(1分)
CaCl2+CO2↑+H2O(1分)
1 1
x 0.07
1/x=1/0.07 (1分)
x=0.07
0.07mol×100g/mol= 7g (1分)
7g/10×100%=70% (1分)
答:该大理石中碳酸钙质量分数为70% 4分
②若取该样品10g,充分煅烧,最多可以产生CO2;根据元素守恒可知,生成的二氧化碳的物质的量为0.07mol×44g/mol=3.08g

练习册系列答案
相关题目