题目内容
【题目】金属在生产、生活中有着广泛的应用。
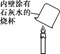
(1)下列金属制品中,利用金属导电性的是_________(填序号)。

(2)工业上,用一氧化碳和赤铁矿(主要成分是Fe2O3)炼铁的化学方程式为_________,计算含氧化铁160t的赤铁矿,理论上能冶炼出纯铁的质量为_________t。
【答案】C Fe2O3+3CO![]() 2 Fe+3CO2 112
2 Fe+3CO2 112
【解析】
(1) A. 黄金饰品是利用金属具有美丽光泽的性质,此选项不符合题意;B.家用铁锅是利用铁具有良好导热性的性质,此选项不符合题意;C.铜丝作电线是利用铜具有良好导电性的性质,此选项符合题意。故选C。
(2)工业上,用一氧化碳和赤铁矿炼铁的化学方程式为:Fe2O3+3CO![]() 2Fe+3CO2
2Fe+3CO2
设能冶炼出纯铁的质量为x。
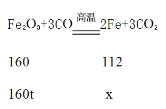
![]() =
=![]() ,解得x=112t
,解得x=112t

【题目】下列实验设计不能达到实验目的的是( )
选项 | A | B | C | D |
实验设计 |
|
|
|
|
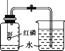
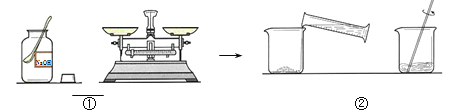
实验目的 | 探究二氧化锰能否加快过氧化氢分解 | 探究石蜡燃烧后是否有二氧化碳生成 | 检验氧气是否集满 | 测定空气中氧气的含量 |
A. A B. B C. C D. D
【题目】钙元素对人类生命和生活具有重要意义,含钙的物质是中学化学研究的重要内容。
(1)牛奶中的钙主要以磷酸钙(Ca3(PO4)2 的形式存在,磷酸钙中磷元素的化合价为_____价。
(2)生石灰溶于水可制得熟石灰,该反应过程中能量的变化是_____(填“吸热”或“放热”)。
(3)氢化钙固体是登山运动员常用的能源提供剂某研究小组的同学通过查阅资料得知:氢化钙(CaH2)遇水反应生成氢氧化钙和氢气。该研究小组的同学把一定量的氢化钙加入到碳酸钠溶液中,充分反应后过滤,得到滤渣和滤液,经检验滤渣的成分是碳酸钙。
(提出问题)滤液中溶质的成分是什么?
猜想一:氢氧化钠
猜想二:氢氧化钠、氢氧化钙
猜想三:氢氧化钠、碳酸钠
猜想四:氢氧化钠、碳酸钠、氢氧化钙
经过讨论,大家一致认为猜想四不合理,请用化学方程式说明理由_____。
(实验验证)
实验 | 现象 | 结论 |
①取少量滤液,向其中滴加少量碳酸钠溶液 | 无明显现象 | 猜想_____不成立 |
②另取少量滤液,向其中滴加足量稀盐酸 | _____ | 猜想三成立 |
(反思与拓展)
①要证明猜想三成立,也可以另取少量滤液,向其中滴加_____。
②在分析化学反应后所得物质的成分时,除考虑生成物外还需考虑_____。
③登山运动员携带氢化钙作为能源提供剂与携带氢气相比,其优点是_____(写一条即可)。