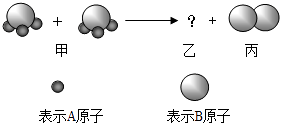
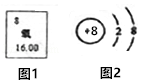
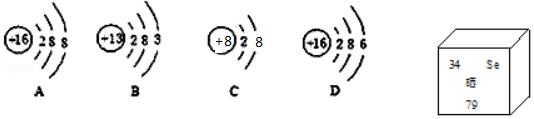题目内容
【题目】某学习小组欲测定刚配制的BaCl2溶液中溶质的质量分数,采取下列两种方法: 方法1:取100gBaCl2溶液,加入适量的AgNO3溶液,两者恰好完全反应,并测得生成AgCl沉淀的质量为m1g;
方法2:取100gBaCl2溶液,加入m2g溶质的质量分数为a%的Na2SO4溶液,恰好使BaCl2溶液完全沉淀;
已知相关物质的相对分子质量:BaCl2=208 Na2SO4=142 AgCl=143.5
(1)请任选一种方法计算该BaCl2溶液中溶质的质量分数(写出详细的计算过程);
(2)如果采取上述两种方法,可推知a=(用含m1、m2的代数式表示)
【答案】
(1)解:设100g氯化钡溶液中溶质的质量为x
方法1:
BaCl2+2AgNO3= | 2AgCl↓+Ba(NO3)2 |
208 | 287 |
x | m1g |
![]() =
= ![]()
x= ![]()
该BaCl2溶液中溶质的质量分数为 ![]() ×100%=
×100%= ![]() ×100%
×100%
方法2:
m2g溶质的质量分数为a%的Na2SO4溶液中溶质的质量为a%×m2g
BaCl2+ | Na2SO4=BaSO4↓+2NaCl |
208 | 142 |
x | a%×m2g |
![]() =
= ![]()
x= ![]() ×a%×m2g
×a%×m2g
该BaCl2溶液中溶质的质量分数为 ![]() ×100%=
×100%= ![]() ×a%×m2×100%
×a%×m2×100%
由于测定的为同一溶液,所以两者计算结果相等, ![]() ×100%=
×100%= ![]() ×a%×m2×100%
×a%×m2×100%
a= ![]()
(2)![]()
【解析】根据给出的数据和对应的化学方程式求算氯化钡的质量进而求算其质量分数.
【考点精析】通过灵活运用根据化学反应方程式的计算,掌握各物质间质量比=系数×相对分子质量之比即可以解答此题.

【题目】分析处理图表中的信息是学习化学的一种重要方法,如表是NH4Cl和KNO3在不同温度时的溶解度数据:
温度/℃ | 10 | 30 | 50 | 70 | |
溶解度/g | NH4Cl | 33.3 | 41.4 | 50.4 | 55.2 |
KNO3 | 20.9 | 45.8 | 85.5 | 110 | |
根据上述数据,回答下列问题:
(1)从上表可知,50℃时,NH4Cl的溶解度为g.
(2)NH4Cl和KNO3的溶解度受温度影响比较大的物质是(填化学式).
(3)欲配制质量分数为10%的KNO3溶液,需要的玻璃仪器有烧杯、量筒、胶头滴管和
(4)烧杯中A中是60℃时,含有100g水的NH4Cl不饱和溶液,经过如图1的变化过程(在整个过程中,不考虑水分的蒸发),则C烧杯中溶液的质量为g. 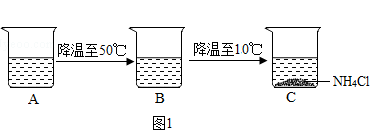
(5)某同学欲验证NH4Cl固体溶于水时吸收热量,设计如图2实验,通过观察到现象得以验证. 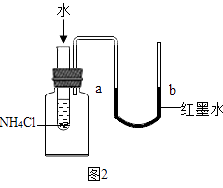
A.a端液面高于b端液面
B.a端液面低于b端液面.