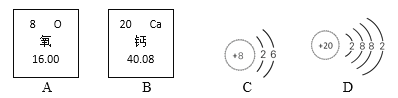
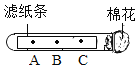
题目内容
【题目】写出下列反应的化学方程式:
(1)碳在氧气中充分燃烧__________。
(2)铁丝在氧气中的燃烧__________。
(3)硫磺在氧气中的燃烧__________。
(4)镁条在氧气中的燃烧__________。
【答案】 C + O2![]() CO2 3Fe + 2O2
CO2 3Fe + 2O2 ![]() Fe3O4 S + O2
Fe3O4 S + O2![]() SO2 2Mg + O2
SO2 2Mg + O2 ![]() 2MgO
2MgO
【解析】
首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤(写、配、注、等)进行书写即可。
(1)碳在氧气中充分燃烧生成二氧化碳,反应的化学方程式为:C + O2![]() CO2;
CO2;
(2)铁在氧气中燃烧生成四氧化三铁,反应的化学方程式为3Fe + 2O2 ![]() Fe3O4;
Fe3O4;
(3)硫磺在氧气中充分燃烧生成二氧化硫,反应的化学方程式为:S + O2![]() SO2;
SO2;
(4)镁条在氧气中燃烧生成二氧化硫,反应的化学方程式为:2Mg + O2 ![]() 2MgO。
2MgO。

【题目】过氧化氢在生产生活中有广泛应用。实验小组对过氧化氢的某些性质进行研究。
Ⅰ.不稳定性
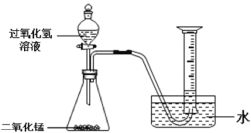
(1)如上图所示进行实验,过氧化氢分解的化学方程式为______。
(2)能用排水法收集O2的原因是______。
(3)探究温度对过氧化氢分解速率的影响。
同学们进行了如下的实验,实验数据如下表:
实验序号 | ① | ② | ③ |
H2O2溶液的浓度 % | 30 | 30 | 30 |
H2O2溶液的体积/mL | 6 | 6 | 6 |
温度/℃ | 20 | 35 | 55 |
MnO2的用量/g | 0 | 0 | 0 |
收集O2的体积/mL | 0 | 1.9 | 7.8 |
反应时间 | 40 min | 40 min | 40 min |
由此得出的结论是______。
Ⅱ.腐蚀性
(查阅资料)H2O2溶液有腐蚀性。
(进行实验)
同学们用铜片设计实验验证H2O2溶液的腐蚀性。(各组实验中H2O2溶液和稀硫酸所用浓度均相同)
将铜片分别浸泡在3种溶液中进行实验,如下表。
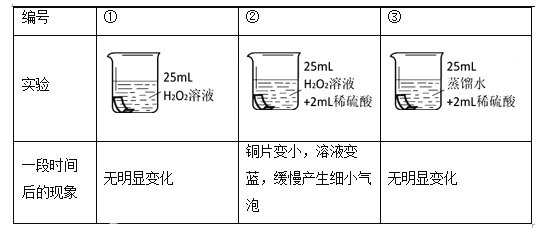
(解释与结论)
(4)实验①的作用是______。
(5)能说明铜片被腐蚀与H2O2溶液和稀硫酸均有关的实验组是______。
(6)铜片被腐蚀的反应如下,补全该反应的化学方程式。Cu + H2O2+ H2SO4=== CuSO4 +□_______/p>