题目内容
【题目】今年春天南方出现了H7N9禽流感,从香料八角中提取的莽草酸(C7H10O5)是合成治疗禽流感药物-达菲的原料。现有17.4g的莽草酸与一定量的氧气在点燃的条件下生成17.6g的:二氧化碳、9g的水和xg的CO。求x的值为_____,参加反应的氧气和莽草酸中的氧元素的质量比为_____,该反应的化学方程式为_____。
【答案】8.4 11:5 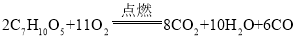
【解析】
①根据质量守恒定律,莽草酸(C7H10O5)中的碳元素通过化学反应转化到二氧化碳和一氧化碳中,
莽草酸(C7H10O5)中碳的质量17.4g×![]() ×100%=8.4g,
×100%=8.4g,
二氧化碳中碳的质量17.6g×![]() ×100%=4.8g,
×100%=4.8g,
那么一氧化碳中碳的质量为8.4g-4.8g=3.6g,
即![]() g×
g×![]() ×100%=3.6g,
×100%=3.6g,
![]() =8.4;
=8.4;
故填8.4g。
②根据质量守恒定律,莽草酸(C7H10O5)跟氧气发生化学反应生成二氧化碳、水和一氧化碳,产物中的氧元素分别来自莽草酸(C7H10O5)和氧气,
莽草酸(C7H10O5)中氧的质量17.4g×![]() ×100%=8g,
×100%=8g,
二氧化碳中氧的质量17.6g×![]() ×100%=12.8g,
×100%=12.8g,
一氧化碳中氧的质量为8.4g×![]() ×100%=4.8g,
×100%=4.8g,
水中氧的质量为9g×![]() ×100%=8g,
×100%=8g,
因此参加反应的氧气质量为12.8g+4.8g+8g-8g=17.6g,
参加反应的氧气和莽草酸中的氧元素的质量比为17.6g:8g=11:5;
故填11:5。
③根据莽草酸(C7H10O5)通过跟氧气发生化学反应生成二氧化碳、水和一氧化碳,故填: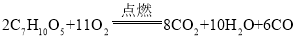 。
。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目