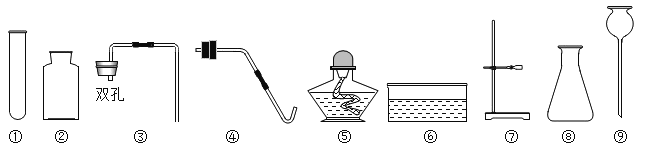
��Ŀ����
����Ŀ��ͬѧ��Χ�ơ�����������ȼ�ա���ʵ��չ������̽�����
�һ��̽����˿��������ȼ��ʱ���������䡱���������京̼���Ĺ�ϵ
��ʵ��̽����
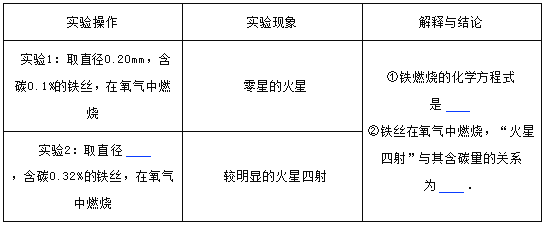
����չ���졿ͬѧ����Ϊ��˿ȼ�յ�������������Ũ���йأ��������ռ���ͬŨ�ȵ������������ʵ�飬������ˮ���ռ�һƿ�������Ϊ90%��������Ԥ��Ӧ���ݻ�Ϊ400mL�ļ���ƿ�м�ˮ��ˮ�����ԼΪ mL��
�����̽����ȼ��ʱ���������ĺ�ɫ�������Ƿ���������
���������ϡ�����Ȼ����������������Ҫ��Fe3O4��Fe2O3���֣�FeO���ױ�����ΪFe2O3����
��������������������ᣮ
��ʵ��̽����
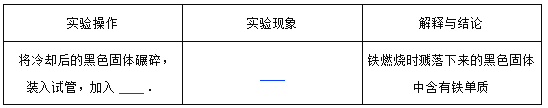
����չ���졿
��֪����������������ˮ�ܷ�Ӧ������������������������÷�Ӧ�Ļ�ѧ����ʽΪ ��
�ɴ˿�֪̽�������Ϊ�˷�ֹ����ƿը�ѣ�Ӧ��ȡ�Ĵ�ʩ�� ��
���𰸡�0.20��3Fe+2O2![]() Fe3O4����̼��Խ�ߣ�����Խ���ԣ�350��ϡ�����������ݲ�����3Fe+4H2O
Fe3O4����̼��Խ�ߣ�����Խ���ԣ�350��ϡ�����������ݲ�����3Fe+4H2O ![]() Fe3O4+4H2���ڼ���ƿ�ײ���һ��ϸɳ
Fe3O4+4H2���ڼ���ƿ�ײ���һ��ϸɳ
��������
����������һ�����ʵ��Ҫע����Ʊ�������֤��˿��ֱ����ͬ������������ȼ���������������������ݱ����ṩ�����ֿ��Կ�������˿�еĺ�̼��Խ�ߣ�����Խ���ԣ����0.20��3Fe+2O2![]() Fe3O4����̼��Խ�ߣ�����Խ���ԣ���չ���죺����ˮ���ռ�һƿ�������Ϊ90%��������Ԥ��Ӧ���ݻ�Ϊ400mL�ļ���ƿ�м�ˮ��������������Ϊ400mL���������������Ϊ��400mL��90%=360mL����ˮ�����Ϊx�����У�400mL��x����+x=360mL��x=350mL�����350����������������ᷴӦ������������Ҫ֤�������������Լ���ϡ���ᣬ�۲쵽�����ݲ�����֤�������������ϡ�����������ݲ�������չ���죺��������������ˮ�ܷ�Ӧ�����������������������÷�Ӧ�Ļ�ѧ����ʽΪ 3Fe+ 4H2O
Fe3O4����̼��Խ�ߣ�����Խ���ԣ���չ���죺����ˮ���ռ�һƿ�������Ϊ90%��������Ԥ��Ӧ���ݻ�Ϊ400mL�ļ���ƿ�м�ˮ��������������Ϊ400mL���������������Ϊ��400mL��90%=360mL����ˮ�����Ϊx�����У�400mL��x����+x=360mL��x=350mL�����350����������������ᷴӦ������������Ҫ֤�������������Լ���ϡ���ᣬ�۲쵽�����ݲ�����֤�������������ϡ�����������ݲ�������չ���죺��������������ˮ�ܷ�Ӧ�����������������������÷�Ӧ�Ļ�ѧ����ʽΪ 3Fe+ 4H2O![]() Fe3O4+4H2��Ϊ�˷�ֹ����ƿը�ѣ�Ӧ��ȡ�Ĵ�ʩ���ڼ���ƿ�ײ���һ��ϸɳ�����3Fe+4H2O
Fe3O4+4H2��Ϊ�˷�ֹ����ƿը�ѣ�Ӧ��ȡ�Ĵ�ʩ���ڼ���ƿ�ײ���һ��ϸɳ�����3Fe+4H2O![]() Fe3O4+4H2���ڼ���ƿ�ײ���һ��ϸɳ
Fe3O4+4H2���ڼ���ƿ�ײ���һ��ϸɳ

 �Ƹ�С״Ԫ�������������ϵ�д�
�Ƹ�С״Ԫ�������������ϵ�д� ����һ������ܼƻ�ϵ�д�
����һ������ܼƻ�ϵ�д�����Ŀ���������ճ����������е��������ʵ���Ͳ���������
��������� | ���� | |
A | ��ů�������������� | �����ڲ����˶� |
B | ϴ�ྫ��ϴ�;������� | ϴ�ྫ���ܽ����� |
C | ����Ʒ�ڳ�ʪ�ط������� | ���������������������ˮ�������ӵĻ�ѧ��Ӧ |
D | ����̿��������ȥζ�� | ����̿���������� |