题目内容
 (2011?玉溪)探究原子结构的奥秘.
(2011?玉溪)探究原子结构的奥秘.【情景提供】19世纪以前,人们一直以为原子是不可分的,直到1887年,汤姆生发现了带负电的电子后,才引起人们对原子结构模型的探索.
【提出问题】电子带负电,原子不带电,说明原子内存在着带正电荷的部分,它们是均匀分布还是集中分布的呢?
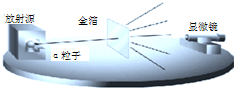
【进行实验】1910年英国科学家卢瑟福进行了著名的α粒子轰击金箔实验.
实验做法如图:
(1)放射源-放射性物质放出α粒子(带正电荷),质量是电子质量的7000倍;
(2)金箔-作为靶子,厚度1um,重叠了3000层左右的原子;
(3)荧光屏-α粒子打在上面发出闪光;
(4)显微镜-通过显微镜观察闪光,且通过360度转动可观察不同角度α粒子的到达情况.
【收集证据】绝大多数α粒子穿过金箔后仍沿原来的方向前进,但是有少数α粒子却发生了较大的偏转,并且有极少数α粒子的偏转超过90°,有的甚至几乎达到180°,像是被金箔弹了回来.
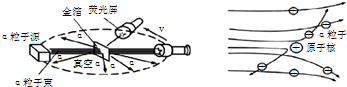
【猜想与假设】α粒子遇到电子后,就像飞行的子弹碰到灰尘一样运动方向不会发生明显的改变,而结果却出乎意料,除非原子的大部分质量集中到了一个很小的结构上,否则大角度的散射是不可能的.
【解释与结论】
(1)若原子质量、正电荷在原子内均匀分布,则极少数α粒子就
不会
不会
(填“会”或“不会”)发生大角度散射.卢瑟福所说的“除非原子的大部分质量集中到了一个很小的结构上”中的“很小的结构”指的是原子核
原子核
.(2)1um金箔包含了3000层金原子,绝大多数α粒子穿过后方向不变,说明
B
B
;A.原子的质量是均匀分布的 B.原子内部绝大部分空间是空的
(3)科学家对原子结构的探究经历了三个过程,通过α粒子散射实验,你认为原子结构为以下的
C
C
.A.

道耳顿模型特点:不可再分的实心球体
B.
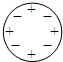
汤姆生模型特点:正负电荷均匀分布
C.
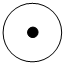
卢瑟福模型特点:核位于原子中心,质量集中在核上.
分析:根据原子结构分析解答;原子的质量主要集中在原子核上,核外有一个非常大的空间.
解答:解:原子是由原子核和核外电子构成的,原子核体积小,质量大,原子的质量主要集中在原子核上,原子核外有一个非常大的空间,核外电子围绕原子核作高速运动.
(1)若原子质量、正电荷在原子内均匀分布,则极少数α粒子就不会发生偏转,大多数发生偏转,而大多数发生了偏转,说明原子的质量主要集中在原子核上,且正电荷不是均匀分布的.
(2)原子核外有一个非常大的空间,使绝大多数α粒子穿过后方向不变
(3)原子结构如图C.
故答案为:(1)不会,原子核(2)B (3)C
(1)若原子质量、正电荷在原子内均匀分布,则极少数α粒子就不会发生偏转,大多数发生偏转,而大多数发生了偏转,说明原子的质量主要集中在原子核上,且正电荷不是均匀分布的.
(2)原子核外有一个非常大的空间,使绝大多数α粒子穿过后方向不变
(3)原子结构如图C.
故答案为:(1)不会,原子核(2)B (3)C
点评:记住并理解原子的结构是解答本题关健.

练习册系列答案
 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案
相关题目
(2011?玉溪)小军家的下水管道堵了.爸爸买回一种“管道通”,使用后堵塞的管道畅通无阻了.小军对此很好奇,于是想探究“管道通”中的物质成分.
【提出问题】“管道通”中的物质是什么?
【查阅资料】主要内容如下.
(1)下水管里的淤积物主要为油污、食物残渣、毛发等.
(2)氢氧化钠是强碱,能去除油污,腐蚀毛发一类的东西.常用于疏通管道.
(3)铝粉为银灰色固体.铝与酸、碱溶液都能反应放出氢气,反应时放出大量热.
①铝与盐酸反应的化学方程式是______.
②铝与氢氧化钠溶液反应的化学方程式是2Al+2NaOH+______═2NaAlO2+3H2↑
【猜想与验证】小军打开一盒“管道通”,内有一袋白色固体颗粒和一袋银灰色粉末.
(1)猜想:白色固体颗粒为氢氧化钠.
结论:白色固体颗粒为氢氧化钠.
(2)猜想:银灰色粉末为铝粉.
结论:银灰色粉末为铝粉.
【应用】
使用管道通时,先将其中银灰色粉状固体添加于被堵塞的管道中,然后再加入白色固体颗粒,倒入一杯水,堵上管道口.一会儿,管道内发生化学反应.根据题目信息,推测管道内的反应现象是______.
【反思】
①老师告诉小军,氢氧化钾和氢氧化钠的性质非常相似.要确认猜想(1)是否正确,还需要学习如何检验钠元素的存在.
②根据本实验分析,使用“管道通”时,应注意的事项有(填一条即可)______.

【提出问题】“管道通”中的物质是什么?
【查阅资料】主要内容如下.
(1)下水管里的淤积物主要为油污、食物残渣、毛发等.
(2)氢氧化钠是强碱,能去除油污,腐蚀毛发一类的东西.常用于疏通管道.
(3)铝粉为银灰色固体.铝与酸、碱溶液都能反应放出氢气,反应时放出大量热.
①铝与盐酸反应的化学方程式是______.
②铝与氢氧化钠溶液反应的化学方程式是2Al+2NaOH+______═2NaAlO2+3H2↑
【猜想与验证】小军打开一盒“管道通”,内有一袋白色固体颗粒和一袋银灰色粉末.
| 实验操作 | 实验现象 |
| 1照下图安装两套仪器. 2 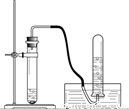 | |
| ②两套仪器中分别依次加入银灰色粉末和稀盐酸;银灰色粉末和______. | 都产生大量无色气体,试管外壁温度明显升高. |
| ③待导管口有气泡均匀持续冒出时,收集1试管气体,验纯.(两套仪器操作相同) | 验纯时的操作和现象:(两套仪器相同) 用拇指堵住集满氢气的试管口,靠近火焰,移开拇指点火,声音很小(或有噗的一声). |
| ④在导管口点燃气体.(两套仪器操作相同) | 都产生淡蓝色火焰. |
结论:白色固体颗粒为氢氧化钠.
(2)猜想:银灰色粉末为铝粉.
实验操作 | 实验现象 |
| ①将几粒白色固体颗粒放在表面皿上,放置一会儿. | 白色固体颗粒表面潮湿并逐渐溶解. |
| ②将几粒白色固体颗粒放入盛有少量水的试管中,并用手触摸试管外壁. | ______. |
| ③向步骤②得到的溶液中放入一段羊毛线,加热一段时间. | 羊毛线逐渐消失. |
【应用】
使用管道通时,先将其中银灰色粉状固体添加于被堵塞的管道中,然后再加入白色固体颗粒,倒入一杯水,堵上管道口.一会儿,管道内发生化学反应.根据题目信息,推测管道内的反应现象是______.
【反思】
①老师告诉小军,氢氧化钾和氢氧化钠的性质非常相似.要确认猜想(1)是否正确,还需要学习如何检验钠元素的存在.
②根据本实验分析,使用“管道通”时,应注意的事项有(填一条即可)______.

(2011?玉溪)小军家的下水管道堵了.爸爸买回一种“管道通”,使用后堵塞的管道畅通无阻了.小军对此很好奇,于是想探究“管道通”中的物质成分.
【提出问题】“管道通”中的物质是什么?
【查阅资料】主要内容如下.
(1)下水管里的淤积物主要为油污、食物残渣、毛发等.
(2)氢氧化钠是强碱,能去除油污,腐蚀毛发一类的东西.常用于疏通管道.
(3)铝粉为银灰色固体.铝与酸、碱溶液都能反应放出氢气,反应时放出大量热.
①铝与盐酸反应的化学方程式是______.
②铝与氢氧化钠溶液反应的化学方程式是2Al+2NaOH+______═2NaAlO2+3H2↑
【猜想与验证】小军打开一盒“管道通”,内有一袋白色固体颗粒和一袋银灰色粉末.
(1)猜想:白色固体颗粒为氢氧化钠.
结论:白色固体颗粒为氢氧化钠.
(2)猜想:银灰色粉末为铝粉.
结论:银灰色粉末为铝粉.
【应用】
使用管道通时,先将其中银灰色粉状固体添加于被堵塞的管道中,然后再加入白色固体颗粒,倒入一杯水,堵上管道口.一会儿,管道内发生化学反应.根据题目信息,推测管道内的反应现象是______.
【反思】
①老师告诉小军,氢氧化钾和氢氧化钠的性质非常相似.要确认猜想(1)是否正确,还需要学习如何检验钠元素的存在.
②根据本实验分析,使用“管道通”时,应注意的事项有(填一条即可)______.

【提出问题】“管道通”中的物质是什么?
【查阅资料】主要内容如下.
(1)下水管里的淤积物主要为油污、食物残渣、毛发等.
(2)氢氧化钠是强碱,能去除油污,腐蚀毛发一类的东西.常用于疏通管道.
(3)铝粉为银灰色固体.铝与酸、碱溶液都能反应放出氢气,反应时放出大量热.
①铝与盐酸反应的化学方程式是______.
②铝与氢氧化钠溶液反应的化学方程式是2Al+2NaOH+______═2NaAlO2+3H2↑
【猜想与验证】小军打开一盒“管道通”,内有一袋白色固体颗粒和一袋银灰色粉末.
| 实验操作 | 实验现象 |
| 1照下图安装两套仪器. 2 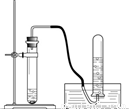 | |
| ②两套仪器中分别依次加入银灰色粉末和稀盐酸;银灰色粉末和______. | 都产生大量无色气体,试管外壁温度明显升高. |
| ③待导管口有气泡均匀持续冒出时,收集1试管气体,验纯.(两套仪器操作相同) | 验纯时的操作和现象:(两套仪器相同) 用拇指堵住集满氢气的试管口,靠近火焰,移开拇指点火,声音很小(或有噗的一声). |
| ④在导管口点燃气体.(两套仪器操作相同) | 都产生淡蓝色火焰. |
结论:白色固体颗粒为氢氧化钠.
(2)猜想:银灰色粉末为铝粉.
实验操作 | 实验现象 |
| ①将几粒白色固体颗粒放在表面皿上,放置一会儿. | 白色固体颗粒表面潮湿并逐渐溶解. |
| ②将几粒白色固体颗粒放入盛有少量水的试管中,并用手触摸试管外壁. | ______. |
| ③向步骤②得到的溶液中放入一段羊毛线,加热一段时间. | 羊毛线逐渐消失. |
【应用】
使用管道通时,先将其中银灰色粉状固体添加于被堵塞的管道中,然后再加入白色固体颗粒,倒入一杯水,堵上管道口.一会儿,管道内发生化学反应.根据题目信息,推测管道内的反应现象是______.
【反思】
①老师告诉小军,氢氧化钾和氢氧化钠的性质非常相似.要确认猜想(1)是否正确,还需要学习如何检验钠元素的存在.
②根据本实验分析,使用“管道通”时,应注意的事项有(填一条即可)______.

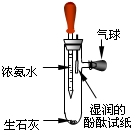 (2011?玉溪)小然同学设计探究分子运动的实验如右图,请按要求完成下列各小题:
(2011?玉溪)小然同学设计探究分子运动的实验如右图,请按要求完成下列各小题: