题目内容
【题目】有关溶液的认识中错误的是( )
A.无色透明的液体是溶液
B.同溶质的饱和溶液一定比它的不饱和溶液要浓
C.![]() 的氯化钠溶液中溶质与溶液质量之比为
的氯化钠溶液中溶质与溶液质量之比为![]()
D.在说到溶液的“饱和”和“不饱和”时,只有指明一定温度、一定量的溶剂这两个前提条件下才有意义
【答案】AB
【解析】
A、均一、稳定的混合物属于溶液,不一定无色,例如硫酸铜溶液为蓝色,故A错;
B、饱和溶液不一定是浓溶液,不饱和溶液不一定是稀溶液,相同温度下,同种溶质的饱和溶液一定比不饱和溶液浓,故B错;
C、![]() 的氯化钠溶液表示在
的氯化钠溶液表示在![]() 氯化钠溶液中含有
氯化钠溶液中含有![]() 氯化钠,溶质与溶液质量之比为
氯化钠,溶质与溶液质量之比为![]() ,故C正确;
,故C正确;
D、饱和溶液是在一定温度下一定量溶剂中不能再继续溶解某溶质的溶液,不饱和溶液则是在同样条件下可以继续溶解某溶质的溶液,由此可知只有指明温度和溶剂的量时,溶液的“饱和”或“不饱和”才有确定的意义,故D正确。
故选AB。

【题目】某兴趣小组在实验室用金属和酸反应来比较铝和锌的金属活动性大小,他们将一块铝片和一块相同质量的锌粒分别放入相同浓度的稀硫酸和稀盐酸中,发现开始时锌粒产生的气体更快,对照金属活动性顺序表,铝排在锌的前面,应该铝更快,为什么会出现这种情况呢?请你一起参与以下探究。
[提出问题]除了“金属活动性、溶液的质量、溶质质量分数”外,还有哪些因素会造成锌比铝产生气体快?
[猜想与假设]猜想1:锌与铝表面的氧化物;
猜想2:酸的种类;
猜想3:温度
[实验探究] (1)按题中开始时小组同学设计的实验方案比较锌、铝的金属活动性是____________(填“合理”或“不合理” )的,原因是_______________________。
(2)请写出铝与稀盐酸反应的化学方程式_______________________。
(3)某同学设计如下实验方案进行实验:
实验步骤 | 实验现象 | 实验结论 |
取表面积相同的锌、铝,分别放入温度相同、浓度相同、体积相同的稀盐酸中 | 锌产生气体快,铝刚开始反应比锌慢,后逐渐快起来 | 猜想1__________( 填“成立"或“不成立”) |
产生这种现象的原因是______________,所以做金属与酸的反应实验时,必要的处理是___________。
[实验拓展]再写一种影响铝与酸反应快慢的因素__________________ (与以上题中提到的影响因素不同),设计合理的实验方案,并写出“实验步骤、现象和结论”。
【题目】如图![]() 是甲、乙、丙三种固体物质的溶解度曲线图。
是甲、乙、丙三种固体物质的溶解度曲线图。
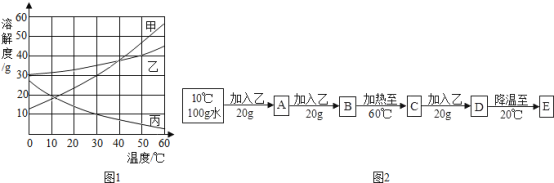
(1)图1中,20℃时,甲、乙、丙三种物质中,溶解度最大的是_____,50℃时,将40g乙物质放入50g水中,充分搅拌,形成溶液的质量为_____。
(2)20℃时,进行了如图![]() 所示的实验:
所示的实验:
①上述溶液中属于不饱和溶液的是_____;
②下列操作能使![]() 中溶液溶质的质量分数发生改变的是_____。
中溶液溶质的质量分数发生改变的是_____。
![]() 、加入20g乙 b、加入100g水 c、升温至40℃ d、加入150g40℃时乙的饱和溶液,再恢复至20℃
、加入20g乙 b、加入100g水 c、升温至40℃ d、加入150g40℃时乙的饱和溶液,再恢复至20℃
(3)如表是NaCI、KNO3在不同温度时的溶解度。
温度/℃ |
|
|
|
|
| |
溶解度 |
|
|
|
|
|
|
|
|
|
|
|
| |
①若要比较KNO3与NaCI在水中的溶解能力,需要控制的量是水的质量和_____。
②若将表中数据在坐标系中绘制成NaCI和KNO3的溶解度曲线,两条曲线的交点对应的温度范围是_____(填序号)。
A 0℃20℃ B 20℃40℃ C 40℃60℃ D 60℃80℃
【题目】某化学兴趣小组的同学把12g石灰石样品和100g稀盐酸(足量)放入烧杯中,在化学反应过程中对烧杯及其中剩余物进行六次称量,记录数据如下表(杂质不溶于水,也不与稀盐酸反应,烧杯的质量为25g)
反应时间(s) | t0 | t1 | t2 | t3 | t4 | t5 |
烧杯和药品质量(g) | 137 | 135 | 133.5 | 133 | 132.6 | 132.6 |
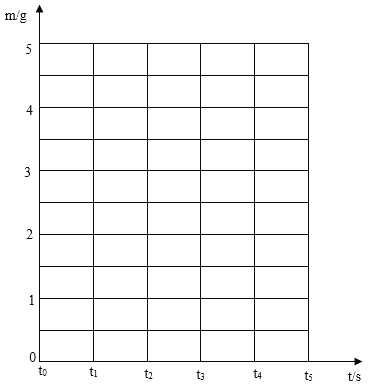
(1)反应共生成了二氧化碳 g.请计算石灰石样品中碳酸钙的质量是多少?
(2)反应完全后所得溶液中氯化钙的溶质质量分数(计算结果精确至0.1% )
(3)请在下面座标图中画出生成的气体质量(m)随时间(t)变化的曲线