��Ŀ����
����Ŀ����֪ͭ���Ժ�Ũ���ᷢ�����·�Ӧ��Cu + 4HNO3(Ũ) = Cu(NO3)2 + 2H2O + 2NO2����ʵ���ҿ���ͨ���÷�Ӧ��ȡ�����������塣NO2��һ�ֺ���ɫ���壬�ܶȱȿ������ܺ�ˮ��Ӧ��NO��NO2���ǿ�������Ⱦ��ָ�������װ�ã�
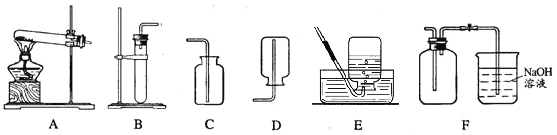
��1��ijͬѧ����ʵ��ʱ����ʧȥ��ǩ��Ũ�����Ũ���ᣬ������ֳ�Ũ���
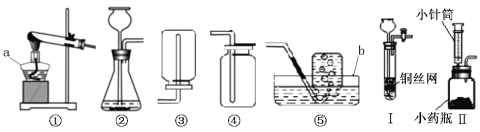
��2����ȡNO2�ķ������ռ�װ��Ӧ�ֱ�ѡ�� �� ����д��������ѡ��ķ���װ����ȡ��һ������ķ�Ӧ����ʽ��
��3�����ŷ�Ӧ�Ľ����ܲ���NO���壬����Ϳ��ܵ�ԭ��
��4����֪NO�ܶȱȿ����Դ�������ˮ��NO����������Ӧ����NO2��Ӧѡ��װ�� �ռ�NO����д��NO��������Ӧ�Ļ�ѧ����ʽ��
��5��ijͬѧ����ʵ���Ϊ���շ�Һ�еĽ���ͭ�����Һ�м���28g��м��ǡ����ȫ��Ӧ���������յ���ͭ��������
���𰸡���1��װ����ɫƿ�����Ũ����
��2��B F 2H2O2MnO22H2O+O2����CaCO3 + 2HCl = CaCl2 + H2O + CO2��
��3������Ũ�������ĺ�ˮ��������Ũ�����ϡ��ͭ��ϡ���ᷴӦ����NO
��4��E 2NO + O2 = 2NO2 ��5��32g
��������
�����������1��Ũ��������ֽ⣬��ʢװ����ɫƿ����ֳ�Ũ����ķ������ǣ�װ����ɫƿ�����Ũ����
��2����ȡ����ķ���װ��ѡ�����ݣ���Ӧ���״̬�ͷ�Ӧ�������ռ�װ��ѡ�����ݣ�������ܶȺ��ܽ��ԣ���ȡNO2���ù���ͭ��Һ��Ũ�����ڳ����·�Ӧ����ѡ����װ��B������NO2�ܶȱȿ������ܺ�ˮ��Ӧ����NO2�ǿ�������Ⱦ���ֻ�ܲ��������ſ������ռ���ͬʱ��Ҫ����β����������ѡװ��F����Һ���·���װ����ȡ��һ������ķ�Ӧ����ʽ��2H2O2MnO22H2O+O2����CaCO3 + 2HCl = CaCl2 + H2O + CO2��
��3�����ŷ�Ӧ�Ľ����ܲ���NO���壬���ܵ�ԭ���ǣ�����Ũ�������ĺ�ˮ��������Ũ�����ϡ��ͭ��ϡ���ᷴӦ����NO
��4�����ݣ�2���ķ�������֪NO�ܶȱȿ����Դ�������ˮ��NO����������Ӧ����NO2��Ӧѡ��װ��E�ռ�NO��NO��������Ӧ����NO2�Ļ�ѧ����ʽ��2NO + O2 = 2NO2
��5��Ϊ���շ�Һ�еĽ���ͭ��������м�ķ�Ӧ����ʽ��Fe + Cu(NO3)2 = Fe(NO3)2 + Cu�����ݷ���ʽ��Fe��Cu��������ϵ������������յ���ͭ������
�⣺����յ���ͭ������Ϊx
Fe + Cu(NO3)2 = Fe(NO3)2 + Cu
56 64
28g x
56/28g = 34/x x=32g
������յ���ͭ������Ϊ32g

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�