题目内容
工业上以用石灰石、水和碳酸钠为原料制取烧碱,请写出制取过程中发生反应的化学方程式.
烧碱的成分是NaOH,石灰石、水和碳酸钠哪一物质与其它物质反应,可生成NaOH,应该是碳酸钠,碳酸钠和石灰石不能直接反应,而石灰石的主要成分是CaCO3,经过高温可得到CaO,方程式为CaCO3
CaO+CO2↑;CaO与水反应可得到Ca(OH)2,方程式为CaO+H2O═Ca(OH)2;Ca(OH)2与Na2CO3反应正好生成NaOH,就是烧碱,方程式为Ca(OH)2+Na2CO3═CaCO3↓+2NaOH.
故答案为:(1)CaCO3
CaO+CO2↑(1分);(2)CaO+H2O═Ca(OH)2(1分);
(3)Ca(OH)2+Na2CO3═CaCO3↓+2NaOH(1分).
| ||
故答案为:(1)CaCO3
| ||
(3)Ca(OH)2+Na2CO3═CaCO3↓+2NaOH(1分).

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
(1)碳酸钠是玻璃、造纸、肥皂、洗涤剂、纺织、制革等工业的重要原料,它属于
(填“酸”、“碱”或“盐”),它的俗名叫纯碱的原因是 .
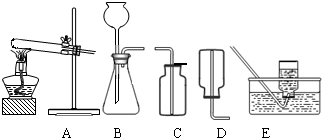
(2)无水碳酸钠的工业制法主要有氨碱法和联合制碱法两种.氨碱法即以食盐(氯化钠)、石灰石(经煅烧生成生石灰和二氧化碳)、氨气(极易溶于水)为原料来制取纯碱.工业上是用N2和H2在高温、高压和催化剂条件下合成氨的.实验室一般用氯化铵和消石灰共热来制备少量的氨气,该反应的化学方程式为 ,制取和收集氨气可用下图中的 和 装置.
(3)某海洋化工集团用氨碱法生产的纯碱产品中含有少量氯化钠杂质,其产品包装袋上注明:碳酸钠≥96%.为测定该产品中含碳酸钠的质量分数,进行了以下实验,取11.0g纯碱样品放入烧杯中,称得烧杯及所盛纯碱样品的总质量为158.0g,再把100g稀盐酸平均分成四份依次加入样品中,每次均充分反应.实验数据记录如下:
请你据此分析计算:
①第一次加入稀盐酸充分反应后,生成二氧化碳的质量是 g.
②该产品中碳酸钠的质量分数是否合格?(要求写出计算过程,结果精确到0.1%)
(2)无水碳酸钠的工业制法主要有氨碱法和联合制碱法两种.氨碱法即以食盐(氯化钠)、石灰石(经煅烧生成生石灰和二氧化碳)、氨气(极易溶于水)为原料来制取纯碱.工业上是用N2和H2在高温、高压和催化剂条件下合成氨的.实验室一般用氯化铵和消石灰共热来制备少量的氨气,该反应的化学方程式为

(3)某海洋化工集团用氨碱法生产的纯碱产品中含有少量氯化钠杂质,其产品包装袋上注明:碳酸钠≥96%.为测定该产品中含碳酸钠的质量分数,进行了以下实验,取11.0g纯碱样品放入烧杯中,称得烧杯及所盛纯碱样品的总质量为158.0g,再把100g稀盐酸平均分成四份依次加入样品中,每次均充分反应.实验数据记录如下:
| 所加盐酸的次数 | 第一次 | 第二次 | 第三次 | 第四次 |
| 烧杯及所盛物质的总质量/g | 181.2 | 204.4 | 228.6 | 253.6 |
①第一次加入稀盐酸充分反应后,生成二氧化碳的质量是
②该产品中碳酸钠的质量分数是否合格?(要求写出计算过程,结果精确到0.1%)