题目内容
【题目】烧杯中盛有CuCl2和HCl的混合溶液100g,向其中滴加10%的NaOH溶液,烧杯中溶液的质量与滴加溶液的质量关系如图所示。下列说法正确的是( )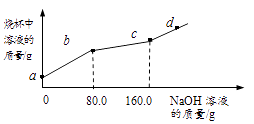
A.ab段反应产生蓝色沉淀
B.bc段溶液增加70.2g
C.c点对应的溶质质量分数为4.9%
D.d点溶液中溶质有2中,且PH>7
【答案】B,D
【解析】A、由图像可知,ab段反应是氢氧化钠先和稀盐酸反应生成氯化钠和水,A不符合题意;
B、由题意可知:与氯化铜反应的氢氧化钠的质量为:(160.0-80.0)g×10%=8.0g
设生成氢氧化铜的质量为x,生成氯化钠的质量为y
CuCl2+ | 2NaOH= | Cu(OH) 2↓+ | 2NaCl |
80 | 98 | 117 | |
8.0g | x | y |
![]()
x=9.8g
y=11.7g
bc段溶液增加的质量为:80g-9.8g=70.2g,B符合题意;
C、设氢氧化钠与盐酸反应生成氯化钠的质量为z
HCl+ | NaOH= | NaCl+H2O |
40 | 58.5 | |
80g | z |
![]()
z=11.7g
c点对应的溶质质量分数为: ![]() =9.3%,C不符合题意;
=9.3%,C不符合题意;
D、d点溶液中溶质有过量的氢氧化钠和生成的氯化钠且PH>7,D符合题意.
故答案为:BD.
烧杯中盛有CuCl2和HCl的混合溶液100g,向其中滴加10%的NaOH溶液,氢氧化钠先和稀盐酸反应生成氯化钠和水,当稀盐酸反应完后,再与氯化铜反应,生成氢氧化铜沉淀和氯化钠,据此分析判断.

练习册系列答案
相关题目
