题目内容
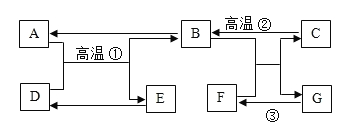
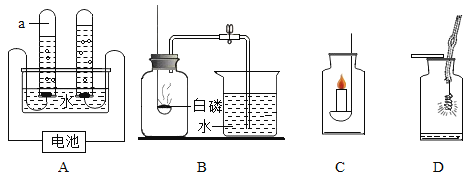
【题目】如图是实验室制取并验证某种气体化学性质的有关装置,回答下列问题:
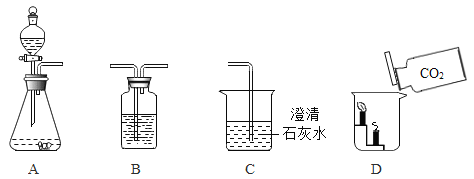
(1)组装好装置A后,制取气体前首先应进行的操作是_____。
(2)A装置可用来制取某些气体,写出其中一个反应的化学方程式_____。若A、C连接,验证某气体的性质,则C中观察到的现象是_____。若A与B连接,则B中紫色石蕊试液变______色。B装置还可用于______。
(3)若将收集的气体进行D操作,则D中的现象是____。
【答案】检查装置气密性 ![]() 澄清石灰水变浑浊 红 干燥气体 烧杯底部的蜡烛先熄灭,上面的蜡烛后熄灭
澄清石灰水变浑浊 红 干燥气体 烧杯底部的蜡烛先熄灭,上面的蜡烛后熄灭
【解析】
碳酸钙和稀盐酸生成氯化钙、水和二氧化碳,二氧化碳和水反应生成碳酸。
(1)组装好装置A后,制取气体前首先应进行的操作是检查装置气密性。
(2)A装置可用来制取某些气体,为固液常温型装置,可以制取二氧化碳,反应为碳酸钙和稀盐酸生成氯化钙、水和二氧化碳,故反应的化学方程式为![]() 。二氧化碳能使澄清石灰水变浑浊,若A、C连接,验证某气体的性质,为验证二氧化碳,则C中观察到的现象是澄清石灰水变浑浊。若A与B连接,二氧化碳和水反应生成碳酸,显酸性,能使紫色石蕊试液变红色,则B中紫色石蕊试液变红色。B装置放入浓硫酸,利用浓硫酸的吸水性干燥气体,故还可用于干燥气体。
。二氧化碳能使澄清石灰水变浑浊,若A、C连接,验证某气体的性质,为验证二氧化碳,则C中观察到的现象是澄清石灰水变浑浊。若A与B连接,二氧化碳和水反应生成碳酸,显酸性,能使紫色石蕊试液变红色,则B中紫色石蕊试液变红色。B装置放入浓硫酸,利用浓硫酸的吸水性干燥气体,故还可用于干燥气体。
(3)若将收集的气体进行D操作,二氧化碳的密度比空气大,不燃烧,不支持燃烧,则D中的现象是烧杯底部的蜡烛先熄灭,上面的蜡烛后熄灭。

 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案【题目】硼镁泥是一种工业废料,主要成份是MgO(占40%),还有CaO、MnO、Fe2O3、FeO、Al2O3、SiO2等杂质。以硼镁泥为原料制取的硫酸镁,可用于印染、造纸、医药等工业。从硼镁泥中提取MgSO4·7H2O的简要工业流程如下:
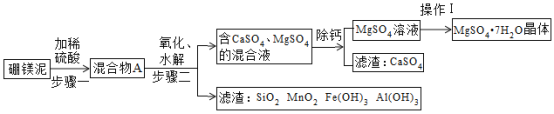
根据题意回答下列问题:
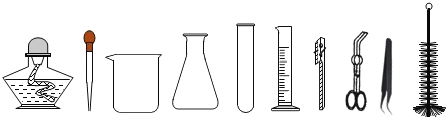
(1)实验中需要用98%的浓硫酸(p=1.84g/mL)来配制一定浓度的稀硫酸。下列所给的仪器中,属于配制过程中必须使用的有_____________(填写选项字母)。
A 普通漏斗
B 蒸发皿
C 量筒
D 烧杯
E 玻璃棒
F 药匙
(2)混合物A中,除了Mg2+、Ca2+、Mn2+、Fe2+,还含有的金属阳离子有______________(填离子符号)。
(3)经过步骤二的过程,化合价发生变化的两种金属元素是______________(填元素符号)。
(4)已知MgSO4、CaSO4溶解度如下表:
温度(℃) | 40 | 50 | 60 | 70 |
MgSO4 | 30.9 | 33.4 | 35.6 | 36.9 |
CaSO4 | 0.210 | 0.207 | 0.201 | 0.193 |
①从表中数据可以总结出CaSO4溶解度随温度的变化趋势是___________________。
②“除钙”是将MgSO4和CaSO4混合溶液中的CaSO4除去,根据上表数据分析,“除钙”适宜的温度是______________(填“较低温度”或“较高温度”)。
(5)“操作I”是将滤液继续蒸发浓缩,冷却结晶,________________,便得到MgSO4·7H2O。
【题目】在实验室,小明将稀盐酸倒入Ba(OH)2溶液中得到溶液甲,相关实验探究如下。
(提出问题)充分反应后所得甲溶液中的溶质是什么?
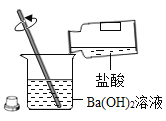
(合理猜想)(1)氯化钡
(2)氯化钡和盐酸
(3)_____________________。
(实验方案)(4)探究甲溶液中是否含有盐酸?
实验 | 操作 | 现象 | 结论 |
① | 取少量甲溶液于试管中, ______________________。 | 没有气泡产生 | 甲中不含盐酸 |
(5)探究甲溶液中是否含有氢氧化钡?
实验 | 操作 | 现象与化学方程式 | 结论 |
② | 取少量甲溶液于试管中,滴入适量的氯化铁溶液。 | _________ | 甲中含氢氧化钡 |
③用一种试剂一次性确定甲溶液中是否含有氢氧化钡还可用的试剂是___________________。 A纯碱 B盐酸 C氯化铜 D硫酸钠 | |||
(得出结论)(6)通过上面的实验(4)(5)推测,猜想合理的是_______________________。