题目内容
某兴趣小组的同学为探究金属的化学性质、以及锈蚀的条件进行了以下系列实验,仔细分析后回答下列问题:
(1)实验一:小明按图1所示以“金属表面产生气泡的快慢”为标准来判断锌、铝、铁的活动性强弱,有同学认为不够合理,理由是______.铝与稀盐酸刚接触时反应缓慢,一段时间后剧烈,产生气泡速率随着加快,其原因可能是______.三种金属活动性由强到弱顺序为______.(写元素符号)
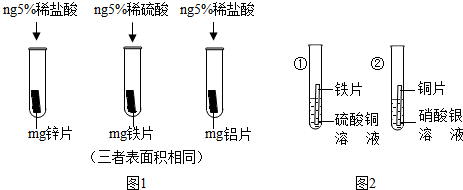
(2)实验二:为探究铁、铜、银三种金属活动性的顺序,小红提出按图2进行两步实验,即可证明三种金属活动性顺序.你认为其方案可行吗?______.(填“可行”或“不可行”)
a.试管①中现象是______;
b.试管②中发生反应的化学方程式为______.
(3)实验三:小芳、小亮两位同学发现铜质眼镜架上出现了一些绿色的锈渍.经查阅资料得知,铜锈的化学成分是碱式碳酸铜[Cu2(OH)2CO3].他们依照钢铁生锈的探究方法设计如下实验(图3所示):
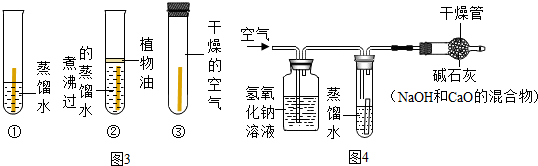
①将光亮铜片部分浸入蒸馏水中;
②将光亮铜片完全浸入煮沸过的蒸馏水中;
③将光亮铜片放在干燥的空气中.
请回答:
a.推测一段时间后会出现铜锈的是______试管内的铜片.(填“①”、“②”或“③”)
b.根据上述实验,小亮同学认为:铜的锈蚀是铜与水、氧气共同作用的结果.你是否同意他的观点?______.(填写“是”或“否”)
c.小芳同学认为要弄清导致铜锈蚀的因素,还应该再补充如图4所示的实验.此实验目的是______,写出铜生锈的化学方程式______.
(1)实验一:小明按图1所示以“金属表面产生气泡的快慢”为标准来判断锌、铝、铁的活动性强弱,有同学认为不够合理,理由是______.铝与稀盐酸刚接触时反应缓慢,一段时间后剧烈,产生气泡速率随着加快,其原因可能是______.三种金属活动性由强到弱顺序为______.(写元素符号)

(2)实验二:为探究铁、铜、银三种金属活动性的顺序,小红提出按图2进行两步实验,即可证明三种金属活动性顺序.你认为其方案可行吗?______.(填“可行”或“不可行”)
a.试管①中现象是______;
b.试管②中发生反应的化学方程式为______.
(3)实验三:小芳、小亮两位同学发现铜质眼镜架上出现了一些绿色的锈渍.经查阅资料得知,铜锈的化学成分是碱式碳酸铜[Cu2(OH)2CO3].他们依照钢铁生锈的探究方法设计如下实验(图3所示):

①将光亮铜片部分浸入蒸馏水中;
②将光亮铜片完全浸入煮沸过的蒸馏水中;
③将光亮铜片放在干燥的空气中.
请回答:
a.推测一段时间后会出现铜锈的是______试管内的铜片.(填“①”、“②”或“③”)
b.根据上述实验,小亮同学认为:铜的锈蚀是铜与水、氧气共同作用的结果.你是否同意他的观点?______.(填写“是”或“否”)
c.小芳同学认为要弄清导致铜锈蚀的因素,还应该再补充如图4所示的实验.此实验目的是______,写出铜生锈的化学方程式______.
解;(1)用控制变量法来探究金属的活动性强弱,金属片的形状、厚薄应该完全相同;应该选择同浓度、同体积的同一种酸;铝片表面有一层致密、结实的氧化铝薄膜,稀盐酸先与氧化铝反应,然后再与铝发生反应产生氢气;根据金属活动性顺序可知,三种金属的活动性顺序是:铝、锌、铁.答案为:选取酸的种类不同;铝表面的氧化膜没有完全去掉;Al、Zn、Fe;
(2)图2的①,铁能置换出硫酸铜中的铜,看到铁丝表面有红色物质出现,硫酸铜溶液是蓝色的,生成的氯化亚铁溶液是浅绿色的;②铜片可以置换出硝酸银中的银,可以证明三种金属的活动性强弱;②中发生的反应是铜与硝酸银反应生成银与硝酸铜.答案为:可行;a.铜片上覆盖一层红色的固体物质,溶液由蓝色逐渐变为浅绿色;b.Cu+2AgNO3=Cu(NO3)2+2Ag;
(3)根据碱式碳酸铜的化学式可以推断出铜的锈蚀与氧气、水和二氧化碳有关,所以①中的铜片一段时间后会锈蚀;补充了一个铜片与水、氧气共存,但是不存在二氧化碳的实验,来验证铜的生锈与二氧化碳有关.该反应是铜、氧气、二氧化碳与水反应生成碱式碳酸铜.故答案为:a.①b.否c.证实二氧化碳也是导致铜生锈的因素之一;2Cu+O2+CO2+H2O=Cu2(OH)2CO3
(2)图2的①,铁能置换出硫酸铜中的铜,看到铁丝表面有红色物质出现,硫酸铜溶液是蓝色的,生成的氯化亚铁溶液是浅绿色的;②铜片可以置换出硝酸银中的银,可以证明三种金属的活动性强弱;②中发生的反应是铜与硝酸银反应生成银与硝酸铜.答案为:可行;a.铜片上覆盖一层红色的固体物质,溶液由蓝色逐渐变为浅绿色;b.Cu+2AgNO3=Cu(NO3)2+2Ag;
(3)根据碱式碳酸铜的化学式可以推断出铜的锈蚀与氧气、水和二氧化碳有关,所以①中的铜片一段时间后会锈蚀;补充了一个铜片与水、氧气共存,但是不存在二氧化碳的实验,来验证铜的生锈与二氧化碳有关.该反应是铜、氧气、二氧化碳与水反应生成碱式碳酸铜.故答案为:a.①b.否c.证实二氧化碳也是导致铜生锈的因素之一;2Cu+O2+CO2+H2O=Cu2(OH)2CO3

练习册系列答案
相关题目