题目内容
【题目】海洋是丰富的化学资源宝库.通过晾晒海水,可以得到含少量泥沙的粗盐.为了得到比较纯净的NaCl(不考虑可溶性杂质),设计了如图所示的实验操作:
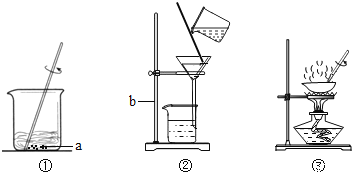
(1)写出图示标号对应的名称:②__________;
(2)操作①②③都用到的仪器是______,在步骤②中该仪器的作用是______;
(3)操作③中看到______时,停止加热,以防液体飞溅;
(4)某同学在进行操作①量水时用俯视量取15mL水,则他量得水的实际体积____15mL(填> 或=或<)
(5)若粗盐的质量为9. 0克,精盐的质量为3. 6克,则该粗盐含有精盐的产率是________,所得到的精盐属于________(填“纯净物”或“混合物”),下列各组同学对造成产率偏高或偏低的原因分析,正确的是_______
A、烧杯里的食盐未溶解完就开始过滤,造成产率低
B、没有蒸发干,精盐中仍有水分,造成产率偏低
C、滤液浑浊就开始蒸发,造成产率偏高
D、蒸发时晶体飞溅,造成产率偏高
【答案】过滤 玻璃棒; 引流 有大量白色固体析出 < 40%; 混合物; AC
【解析】
(1)图中标号对应实验的名称:②过滤;
(2)操作①②③都用到的仪器是玻璃棒,在过滤中玻璃棒的作用是引流;溶解时玻璃棒的作用是搅拌加速溶解;蒸发时玻璃棒的作用是搅拌,使液体受热均匀,防止液体飞溅;
(3)操作③中看到大量晶体析出或有少量液体剩余时,停止加热,以防液体飞溅;
(4)量取液体读数时,要平视凹液面的最低处;仰视读数,读数偏小,实际液体偏多;俯视读数,读数偏大,实际液体偏少。某同学在量水时俯视量取15mL水,则他量得水的实际体积小于15mL;
(5)若粗盐的质量为9. 0克,精盐的质量为3. 6克,则该粗盐含有精盐的产率是3. 6g÷9. 0g×100%=40%,过滤操作只能除掉氯化钠中的难溶性固体,不能除掉其中的可溶性杂质,所得到的精盐属于混合物;粗盐提纯的产率是指提纯所得的氯化钠质量占原粗盐总质量的百分含量。A、烧杯里的食盐未溶解完就开始过滤,导致部分氯化钠未溶解,以固体形式留在滤渣中,所得纯氯化钠偏少,造成产率低,正确;B、没有蒸发干,精盐中仍有水分,导致所得氯化钠的质量偏高,造成产率偏高,错误;C、滤液浑浊,说明难溶性固体没有除尽,将浑浊液体蒸发,得到的氯化钠中有难溶性固体杂质,质量偏大,造成产率偏高,正确;D、蒸发时晶体飞溅,所得氯化钠偏少,造成产率偏低,错误。故选AC。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】一定条件下,甲、乙、丙、丁四种物质在一密闭容器中充分反应,测得反应前后各物质的质量如下表:
物质 | 甲 | 乙 | 丙 | 丁 |
反应前质量/g | 2 | 8 | 30 | 50 |
反应后质量/g | 36 | 8 | 待测 | 22 |
(1)经计算待测数值为____________。
(2)该反应基本类型为 ___________。
(3)该实验中乙为该反应的催化剂,则在化学反应前后乙的______和 ________不发生改变。
(4)已知丙和丁的化学计量数之比是3:1,则丙和丁的相对分子质量之比为___________(填序号)。
A .1﹕14 B.3﹕14 C.12﹕11 D.3﹕5