题目内容
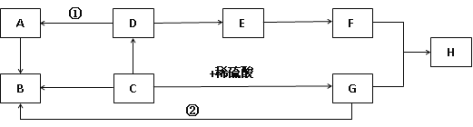
【题目】(5分)根据下列图示回答。
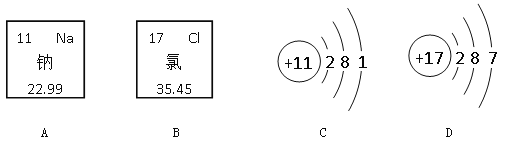
(1)A、B、C、D共表示____种元素,其中属于金属元素的是______(填元素名称)。
(2)Cl在化学反应中容易 (填“得到”或“失去”)电子,形成 (填化学符号)。
(3)钠元素与氯元素形成的化合物的相对分子质量为__________。
【答案】(1)两(两种、2、2种、二、二种均给分) 钠(错别字不给分)(2)得到 Cl— (3)58.44(58.4、58.5、58.45、58均给分)
【解析】
试题分析:(1)决定原子种类的微粒为质子数,故(1)A、B、C、D共表示两种元素,金属元素的原子最外层的电子数小于4个,故其中属于金属元素的是钠元素
(2)Cl在化学反应中容易得到电子,形成Cl—
(3)钠元素与氯元素形成的化合物为NaCl,相对分子质量为58.5。

【题目】(9分)CO2通入NaOH溶液中没有明显现象,CO2与NaOH是否发生了化学反应呢?某化学兴趣小组的同学们对此进行了探究。
【查阅资料】①通常情况下,1体积水溶解1体积的CO2。
②在一定浓度的溶液中,有微溶物生成的复分解反应也能发生。
【实验探究】小红同学设计了下图所示的实验装置(锥形瓶内充满CO2),并进行实验。
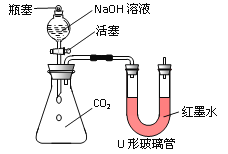
打开瓶塞和活塞,使NaOH溶液快速滴入锥形瓶中,立即关闭活塞(漏斗中仍有溶液剩余),观察到U形管左侧的红墨水液面______(填“升高”、“降低”或“不移动”),小红根据现象判断CO2和NaOH发生了反应,理由是___________。请根据初中化学知识写出CO2与NaOH溶液反应的化学方程式:____________。
【反思与评价1】小明认为小红的实验方案不严密,理由是_______________________。
【拓展实验】兴趣小组的同学们为此又设计了下表所示的两种方法,进一步探究。请填写表中的空格。
实验方法 | 操作过程 | 现象 | 实验结论 |
方法一 | 取小红实验后锥形瓶内的溶液适量,加入足量CaCl2溶液 | 有白色沉淀生成 | CO2与NaOH发生了反应 |
方法二 | 取小红实验后锥形瓶内的溶液适量,加入足量稀硫酸 | ______________ |
【反思与评价2】同学们经过讨论,认为【拓展实验】的______(填“方法一”或“方法二”)依然不严密,理由是___________________________(用化学方程式表示)。