题目内容
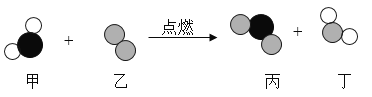
【题目】如下图是某反应前后分子种类变化的微观示意图。下列说法正确的是

A.反应前后分子个数不变B.反应中涉及到3种氧化物
C.反应中甲、乙分子个数比为1:1D.丙的相对分子质量为64
【答案】D
【解析】
由微观示意图可知,甲、乙、丙、丁分别为H2S、O2、SO2、H2O,化学方程式为2H2S+3O2![]() 2SO2+2H2O。
2SO2+2H2O。
A、由分析可知化学方程式为2H2S+3O2![]() 2SO2+2H2O,化学反应前后分子数改变,故A错。
2SO2+2H2O,化学反应前后分子数改变,故A错。
B、由分析可知甲、乙、丙、丁分别为H2S、O2、SO2、H2O,丙、丁有两种元素组成并且含有氧元素为氧化物,涉及到两种氧化物,选项错误。
C、由分析可知化学方程式为2H2S+3O2![]() 2SO2+2H2O,甲、乙分子个数比为2:3,故C错。
2SO2+2H2O,甲、乙分子个数比为2:3,故C错。
D、由分析可知丙为二氧化硫相对分子质量32×1+16×2=64,故D正确。
故选:D。

 名校课堂系列答案
名校课堂系列答案【题目】在学习金属活动性顺序时,老师说:“排在前面的金属能将后面的金属从他们的盐溶液中置换出来,但是K、Ca、Na除外,因为K、Ca、Na能与溶液中的水发生反应”。对这个问题,课外小组的同学很感兴趣,展开了金属与水反应的探究。
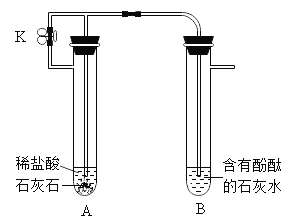
探究I: 探究钠、镁能否与水反应
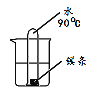
分别将等质量的镁条打磨干净投入25oC和100oC的沸水中,观察记录实验现象:
实验序号 | ① | ② | ③ |
实验装置 |
|
|
|
实验 现象 | 钠浮在水面上,不断跳动,很快收集到一试管气体,金属钠最后消失 | 有细小气泡,镁条逐渐变灰黑色,10分钟后无明显变化 | 有较大气泡冒出,镁条逐渐变灰黑。约5分钟后,无明显现象 |
向烧杯中滴加酚酞,变红 | 收集约5mL气体,取出试管,将燃着的木条伸入试管中,有尖锐的爆鸣声 |
发现问题:镁条为什么不能持续冒出气泡。
查阅资料: Mg(OH)2难溶于水;NH4+和HCO3-可以加快Mg与水反应。
探究II:探究NH4+和HCO3-对Mg与水反应是否有促进作用
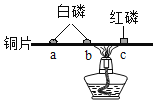
用探究I与水反应后的Mg条与4种盐溶液进行对比实验,结果如下。
实验序号 | a | b | c | d |
盐溶液(浓度相同) | NH4Cl | NaHCO3 | NaCl | NH4HCO3 |
5.1 | 8.3 | 7 | 7.8 | |
30min时产生气体体积(mL) | 1.5 | 0.7 | <0.1 | 1.4 |
气体的主要成分 | H2 | |||
30min时镁条表面情况 | 大量固体附着(固体可溶于盐酸) | |||
根据以上探究回答下列问题:
(1)钠与水反应后的液体显__________(填“酸性”、“碱性”、“中性”)。
(2)由探究I推出钠具有的一条物理性质是__________。
(3)证明镁条能与水发生反应的证据是__________。
(4)通过以上探究得出Mg与水反应的化学方程式为__________。
(5探究II中能够说明HCO3-对Mg与水反应起促进作用的证据是_________。
(6)分析探究全过程,得出影响金属与水反应速率的因素有__________(至少答两点)。