题目内容
早在西汉时期,我国就用铁与硫酸铜溶液反应制取铜,称为“湿法炼铜”。
(1)请写出“湿法炼铜”的化学方程式???????????????????????????? 。
(2)若用该方法制得铜32 g,反应的铁的质量为????? g,若同时消耗了500 g硫酸铜溶液,则该硫酸铜溶液中硫酸铜的质量分数为? ????? %。
【答案】
(1)Fe+CuSO4=Cu+FeSO4 (2)28 16
【解析】本题考查化学方程式的书写和溶液的有关计算。题目中涉及的化学反应为:Fe+CuSO4=Cu+FeSO4,把铜的质量32 g代入化学方程式求出参加反应的铁和硫酸铜的质量,然后据硫酸铜和硫酸铜溶液的质量求出硫酸铜的质量分数。
解:设参加反应铁的质量为x,500 g硫酸铜溶液中硫酸铜的质量为y。
Fe+CuSO4=Cu+FeSO4
56?? 160???? 64?
x???? y????? 32 g
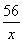 =
=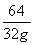
x=28 g
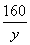 =
=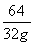
y=80 g
硫酸铜溶液中硫酸铜的质量分数为:
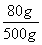 ×100%=16%
×100%=16%

练习册系列答案
 一线名师权威作业本系列答案
一线名师权威作业本系列答案
相关题目