题目内容
新型材料纳米级Fe粉具有广泛的用途,它比普通Fe粉更易与氧气反应,其制备工艺流程如下图所示:
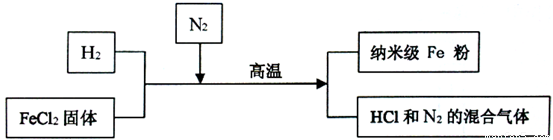
请回答下列问题:
(1)纳米级Fe粉在氧气中能自发燃烧生成黑色固体,此黑色固体的化学式为 。
(2)请补充完成上述制备工艺的化学方程式:H2 +FeCl2高温Fe+ 。 在制备纳米级Fe粉的工艺流程中,N2的作用是 。
(3)研究人员发现最后制得的纳米级Fe粉样品中混有少量的FeCl2杂质。
①为除去样品中的杂质,在无氧环境下,先加 溶解,然后再 、洗涤、烘干.
②取样品20g,加入足量的盐酸,生成氢气0.7g。请计算该样品中单质Fe的质量分数。
(请写出计算过程)____ 。
(1)Fe3O4.(2)2HCl. 催化作用. (3)①水,过滤. ②98%
【解析】试题分析:(1)铁在氧气中燃烧生成的黑色固体为四氧化三铁(Fe3O4)。
(2)根据题意可知,另一种生成物为HCl,所以反应的化学方程式为:H2 +FeCl2高温Fe+2HCl在制备纳米级Fe粉的工艺流程中,N2的作用是催化作用。
(3)①为除去样品中的杂质即除去铁粉中的氯化亚铁,可利用氯化亚铁溶解于水,而铁不溶解于水的性质,使用过滤的方法将其除去。因此应先加水溶解,再过滤。得到滤出的固体为铁粉。然后将固体洗涤、烘干即得到纯净的还原性铁粉。
②中已知量为氢气的质量,未知量为单质铁的质量。可根据反应的化学方程式中二者的关系进行求解。具体的计算过程如下:
解:设参加反应的铁的质量为x,则: 设未知量
Fe+2HCl═FeCl2+H2↑ 写出反应的化学方程式
56 2 标出物质的质量关系
x 0.7g 标出物质的实际质量
56:2=x:0.7g 列比例式
x =19.6g 求解未知量
样品中单质Fe的质量分数为:
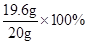 =98%
=98%
考点:科学探究、根据化学方程式的计算
点评:找出计算中的已知未知量,可以根据它们在化学方程式中的质量关系进行计算求解。