题目内容
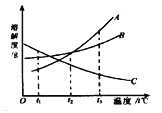
【题目】如图为KNO3的溶解度曲线图,现有M状态(溶剂质量与溶质质量之比为100:30)下的KNO3溶液65g,若要将该溶液经过处理后,刚好得到该温度下的饱和溶液,下列处理方法正确的是( )

A.在t2℃时,将65g溶液倒出去32.5g
B.将65g溶液蒸发掉32.5g的水,再冷却到t2℃
C.将65g溶液的温度从t2℃降低到t1℃
D.在t2℃时,向65g溶液中加入15gKNO3固体并充分溶解
【答案】D
【解析】
试题分析:从图示看:在t2℃时,将65g溶液倒出去32.5g不能变为饱和溶液,因为溶液具有均一性;在t2℃时,向65g溶液中加入15gKNO3固体并充分溶解,因为65克溶液中溶质是15克,溶剂是50克,此时的溶解度是60克,所以50克水中能够溶解30克硝酸钾。故选D.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】某班化学实验课进行酸碱盐的性质实验。
〖实验一〗自制酸碱指示剂
(1)取少量紫包菜和白菜叶剪碎后分别在研钵中捣烂,加入酒精溶液浸泡;用纱布将浸泡出的汁液滤出,观察到紫包菜汁液为紫色,白菜汁液为无色。分别装好待用。
(2)取四支试管分别用NaOH溶液和稀盐酸进行实验,观察到现象如图。

记录如下:
NaOH溶液 | 稀盐酸 | |
紫包菜汁液 | ①绿色 | ②红色 |
白菜汁液 | ③无色 | ④淡黄色 |
你认为两种汁液中,更适合做酸碱指示剂的是 。
(3)再用苹果汁进行相同实验,紫包菜汁液变红色,白菜汁液变淡黄色。则苹果汁溶液显 性。
〖实验二〗探究碱和盐的性质
第一组学生进行CuSO4、NaOH溶液的反应,观察到的现象是 ;该反应的化学方程式为 。
第二组学生进行BaCl2、Na2CO3溶液的反应,反应的化学方程式为 。
〖实验三〗废液再探究
〖实验二〗结束后,两组同学将全部的废液集中倒进一个废液缸中。兴趣小组同学对废液进行过滤,得到无色滤液。
【提出问题】
滤液中含有什么溶质?
【做出猜想】
滤液中一定含有 ,还可能含有BaCl2、NaOH、Na2CO3、Na2SO4中的一种或几种。
【实验探究】
(1)取少量滤液加入试管中,滴加紫包菜汁液,溶液显绿色。
(2)继续加入足量的稀硫酸,溶液变成红色,无气泡和沉淀产生,则滤液中一定没有 。根据(1)(2)判断滤液中一定含有 。
(3)为最终确定该滤液的组成,还需补充的实验是: ,观察到白色沉淀。
【实验结论】 该无色滤液的组成为 。