题目内容
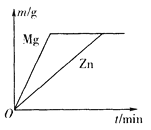
【题目】把一定质量的锌和镁分别投入足量的稀盐酸中,充分反应后,生成氢气的质量关系如下图所示(图中m表示氢气的质量,t表示反应时间),则投入的锌和镁的质量比是 ( )
A. 1:1 B. 24:65 C. 65:24 D. 无法确定
【答案】C
【解析】金属活动顺序表:K Ca Na Mg Al Zn Fe Sn Pb H Cu Hg Ag Pt Au,在金属活动顺序表中,排在氢前边的金属能和酸发生置换反应生成盐和氢气。金属的位置越靠前,金属的活动性越强,和酸反应的速率越快。把一定质量的锌和镁分别投入足量的稀盐酸中,镁的活动性比锌强,所以先反应完,镁和氢气的质量比为24:2,锌和氢气的质量比为65:2,由图可知,最终镁和锌生成氢气一样多,故 投入的锌和镁的质量比是65:24。故选C。

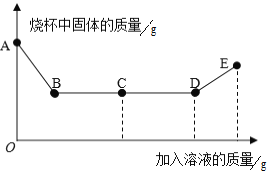
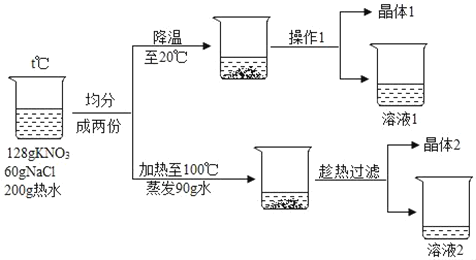
【题目】由128克硝酸钾、60克氯化钠组成的混合物投入200g热水溶解,对该溶液进行如图实验(假设实验过程中无损耗)。
温度(℃) | 10 | 20 | 30 | 40 | 60 | 80 | 100 | |
溶解度 | 硝酸钾 | 20.9 | 31.6 | 45.8 | 64 | 110 | 169 | 246 |
氯化钠 | 35.8 | 36 | 36.3 | 35.4 | 37 | 38.4 | 39.8 | |
(1)两种物质溶解在水中,用玻璃棒搅拌的目的是_____。
(2)实验时温度t的范围为_____。
(3)操作1用到的实验仪器有_____。
A酒精灯 B铁架台 C漏斗 D玻璃棒 E蒸发皿
(4)定量叙述晶体1的组成_____。
(5)溶液2为_____(填物质名称)的饱和溶液。
(6)关于溶液中NaC1的质量分数:溶液1_____溶液2(选填“>“、“<”或“=“)
(7)关于上述实验说法错误的是_____。
A晶体1与晶体2比较,晶体1中KNO3的纯度更高
B溶液1中KNO3为饱和溶液,NaCl为不饱和溶液
C溶液1恒温蒸发90g水后,与溶液2的成分相同
D溶液2将水蒸干就可得到纯净的KNO3固体
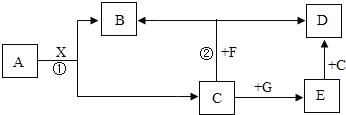
【题目】某白色固体可能由BaC12、NaOH、Na2CO3、Na2SO4;中的一种或几种物质组成,某兴趣小组的同学为确定该白色固体的成分,进行了如下的实验探究,请你参与并回答相关问题。
I.初步探究:小金同学设计的实验过程及现象如图所示。
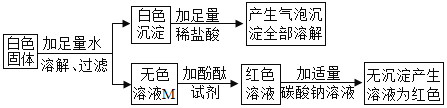
(查阅资料)BaC12溶液显中性。
(初步结沦)(1)原白色固体中一定有的物质是_____,一定没有的物质是_____。白色沉淀溶解的化学方程式是_____。
(2)M溶液中的溶质一定有_____,一定没有氯化钡。
(交流讨论)小英同学认为:无色溶液M变红色,说明溶液M中含有碱性物质,但不能由此推导出原固体物质中是否含有氢氧化钠。若要进一步确定,需对溶液M继续进行探究。为此同学们进行了如下的探究:
Ⅱ.继续探究:
(提出问题)无色溶液M中有氢氧化钠吗?
(猜想与假设)猜想一:有NaOH
猜想二:没有NaOH
(探究与结论)
实验步骤 | 实验现象 | 实验结论 |
A.取无色溶液M于试管中,加入过量的氯化钡溶液,振荡,静置 | _____ | 证明溶液M中有碳酸钠并被除尽 |
B.取实验A所得上层清液于试管中,加入_____。 | _____ | 猜想一正确 |
在老师的指导下,同学们通过交流、讨论、实验,圆满地完成了这次探究活动。