题目内容
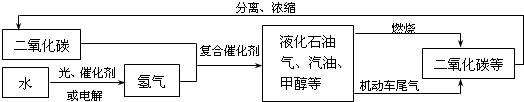
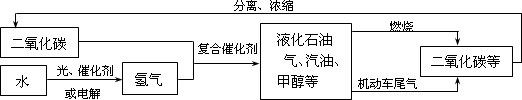
在化学变化中,参加化学反应的物质总质量与生成物的总质量相等,且化学反应中各反应物与生成物之间的质量比是一定的.某中学化学小组用加热氯酸钾与二氧化锰制取氧气,实验测得相关数据如图所示:

(1)剩余的混合物中二氧化锰的质量为
(2)反应生成氧气的质量为
(3)根据化学方程式进行计算,现在需要9.6 克氧气,求需要加热多少克氯酸钾完全反应才能够得到?

(1)剩余的混合物中二氧化锰的质量为
1.0
1.0
克,二氧化锰在反应中的作用是催化作用
催化作用
;(2)反应生成氧气的质量为
19.2
19.2
g.(3)根据化学方程式进行计算,现在需要9.6 克氧气,求需要加热多少克氯酸钾完全反应才能够得到?
分析:(1)根据催化剂的特点进行分析;
(2)根据质量守恒定律分析生成氧气的质量;
(3)根据氯酸钾分解的方程式,由氧气的质量可求出氯酸钾的质量.
(2)根据质量守恒定律分析生成氧气的质量;
(3)根据氯酸钾分解的方程式,由氧气的质量可求出氯酸钾的质量.
解答:解:(1)由催化剂的特点可知,催化剂的质量在反应前后不变,剩余的混合物中二氧化锰的质量为1.0 克,二氧化锰在反应中的作用是催化作用;
(2)加热氯酸钾与二氧化锰混合物,生成了氧气,止质量不再减少时,由质量守恒定律可知生成氧气的质量为:49.0g+1.0g-30.8g=19.2g;
(3)设需要加热氯酸钾的质量为X
2KClO3
2KCl+3O2↑
245 96
X 9.6g
=
解得:X=24.5g
答:(1)1.0,催化作用;(2)19.2;(3)需要加热24.5克氯酸钾完全反应才能够得到.
(2)加热氯酸钾与二氧化锰混合物,生成了氧气,止质量不再减少时,由质量守恒定律可知生成氧气的质量为:49.0g+1.0g-30.8g=19.2g;
(3)设需要加热氯酸钾的质量为X
2KClO3
| ||
| △ |
245 96
X 9.6g
| 245 |
| 96 |
| X |
| 9.6g |
答:(1)1.0,催化作用;(2)19.2;(3)需要加热24.5克氯酸钾完全反应才能够得到.
点评:主要考查了根据化学方程式进行相关的计算及质量守恒定律的应用,培养学生的应用知识的能力和解决问题的能力.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目