题目内容
【题目】生产金属镁后的废渣可以综合利用制备光卤石(MgCl2·6H2O)和金属镁,其工业流程如下图所示:
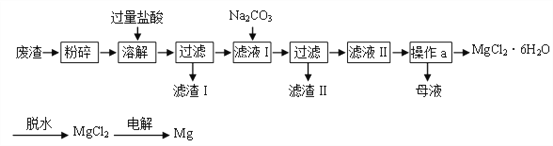
已知:①废渣的主要成份:MgCl2、KCl、MgO、BaCl2、CaCl2、粉尘等杂质。
②MgCO3微溶于水,本题中视为可溶。
回答下列问题:
(1)将废渣粉碎的作用是_______________________。
(2)流程中往滤液I中加入Na2CO3时发生了多个化学反应,请写出其中能够产生气体的那个化学方程式______________________。
(3)滤渣Ⅱ的主要成分____和____;母液的主要成分有3种,分别是MgCl2、____和____。
(4)操作a包含多个操作,分别为______________________过滤,洗涤,干燥。
【答案】 增大接触面积,加快溶解过程反应速率 Na2CO3+2HCl= 2NaCl+H2O+CO2↑ CaCO3 BaCO3 KCl NaCl 蒸发浓缩,冷却结晶
【解析】(1)根据增大接触面积,加快溶解过程反应速率解答;(2)根据盐酸与碳酸钠反应生成氯化钠、水和二氧化碳解答;(3)根据碳酸钠与氯化钡和氯化钙反应生成碳酸钡和碳酸钙的沉淀及废渣粉碎溶解后的溶液中含有氯化镁、氯化钾及过量盐酸与碳酸钠反应生成的氯化钠解答;(4)根据由溶液得到晶体的方法是蒸发结晶解答。(1)将废渣粉碎的作用是增大接触面积,加快溶解过程反应速率;(2)盐酸与碳酸钠反应生成氯化钠、水和二氧化碳,反应的化学方程式为Na2CO3+2HCl= 2NaCl+H2O+CO2↑;(3)废渣粉碎溶解后得到含有氯化钡和氯化钙的溶液,向其中加入碳酸钠溶液,碳酸钠与氯化钡、氯化钙反应生成碳酸钡和碳酸钙的沉淀。故滤渣Ⅱ的主要成分是CaCO3和BaCO3;母液的主要成分有3种,分别是MgCl2、 KCl和NaCl;(4)操作a包含多个操作,分别为蒸发浓缩,冷却结晶、过滤,洗涤,干燥。

 名校课堂系列答案
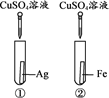
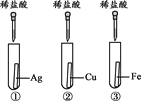
名校课堂系列答案【题目】为探究铁、铜、银三种金属的活动性顺序,设计了A、B两个方案。
方案A | 方案B |
|
|
(1)能验证三种金属活动性顺序的方案是________(填“A”或“B”)。
(2)方案B中,证明铁的活动性比铜强的现象是___________。