题目内容
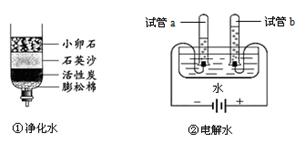
如图是电解水的实验装置图,请根据你所了解的知识填空:
(1)A为 极;
(2)乙中气体的检验方法 。
(3)电解1mol水产生O2的质量为多少克?(写出计算过程)
(1)负
(2)用带火星的木条伸入试管中,发现复燃,证明是氧气
(3)16g
解析试题分析:电解水口诀:正氧负氢,氢二氧一,即与电源正极相连的产生的气体是氧气,与电源负极相连的产生的气体是氢气,并且氢气的体积是氧气体积的2倍,所以(1)从图可以看出甲试管内排开水的体积更多,所以可判断甲产生的是氢气,所以A为负极
(2)试管乙中产生的自然是氧气,检验方法:用带火星的木条伸入试管中,发现复燃,证明是氧气
(3)根据化学方程式:2H2O 2H2↑ + O2↑,已知1mol水,
2H2↑ + O2↑,已知1mol水,
2H2O 2H2↑ + O2↑
2H2↑ + O2↑
2 1
1mol x 2:1=1mol:x
x=0.5
氧气的质量:0.5x32=16
产生的O2质量为16克
考点:电解水的实验,根据化学方程式进行计算

练习册系列答案
相关题目
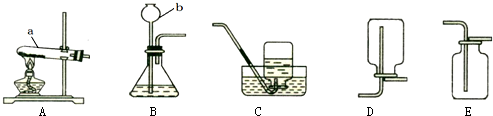
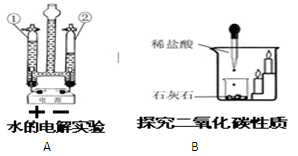
下列是初中化学部分重要的实验或实验装置,请按要求填空:
| A.水的电解实验 | B.测定空气里氧气含量 |
| C.探究二氧化碳性质 | D.气体制备装置 |
(2)B实验如果实验数据小于21%,可能原因是 (写出一点);
(3)C实验说明二氧化碳具有的性质是 ;
(4)选择D装置制取气体的依据是 。
D装置可以制取那些气体 。
 C+2MgO,反应中的氧化剂是(6).该反应中镁带中的镁元素转变为(7)(填“化合”或“游离”)态。
C+2MgO,反应中的氧化剂是(6).该反应中镁带中的镁元素转变为(7)(填“化合”或“游离”)态。