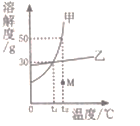
题目内容
【题目】味精的主要成分是谷氨酸钠,易溶于水,其化学式为C5H8NO4Na,与硝酸银溶液不反应。味精中还含有少量的氯化钠(味精中其他成分不考虑),氯化钠与硝酸银溶液发生复分解反应,生成氯化银白色沉淀。回答下列问题:
(1)称取5.0g味精配制成50g溶液,量取蒸馏水的量简规格是__________(填字母)。
A.10mL B. 50mL C.100mL
(2)下图是配制过程,正确的操作顺序为__________(填序号) 。
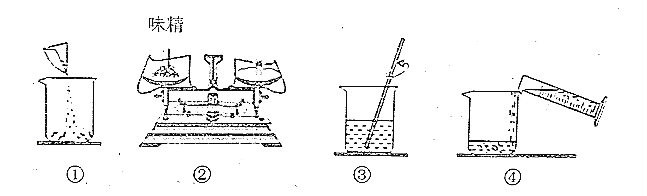
(3)在其他操作均正确的情况下,若配制过程中仰视读取蒸馏水的体积,则所配制溶液中谷氨酸钠的质量分数__________(填“偏大”“偏小”或“无影响”)。
(4)为测定味精中含有氯化钠的质量分数,继续实验:
①向所配制的50g溶液中加入过量的__________溶液(填化学式)充分反应。
②然后进行__________(填操作名称)、洗涤、干燥、称量白色沉淀固体。经精确测定白色沉淀的质量为2.87g,则该味精中氯化钠的质量分数为__________。
【答案】B ②①④③ 偏小 AgNO3 过滤 23.4%
【解析】
由题目的信息可知,(1)根据量筒的使用规则分析;(2)根据配制溶液的步骤分析;(3)根据溶质的质量分数公式分析;(4)①根据氯化钠与硝酸银溶液发生复分解反应,生成氯化银白色沉淀分析;②过滤可以分离固体和液体;结合化学方程式进行计算。
(1)称取5.0g味精配制成50g溶液,需要水的质量=50g-5g=45g,即45mL,量取蒸馏水的量筒规格是50mL;
(2)操作步骤是:计算→称量→溶解→装瓶→贴签→入柜,如图是配制过程,正确的操作顺序为:②①④③;
(3)在其他操作均正确的情况下,若在配制溶液过程中,仰视刻度量取蒸馏水,则所配制溶液的谷氨酸钠质量分数偏小,因为水量多了;
(4)①氯化钠与硝酸银溶液发生反应生成氯化钡和硝酸钠,向所配制的50g溶液中加入过量的硝酸银溶液充分反应,转化为氯化银沉淀;②然后进行过滤、洗涤、干燥、称量氯化银白色沉淀;
解:设氯化钠的质量为x,
NaCl+AgNO3=AgCl↓+NaNO3
58.5143.5
x2.87g
![]()
x=1.17g;
该味精中氯化钠的质量分数=![]() ×100%=23.40%;
×100%=23.40%;
答:该味精中氯化钠的质量分数为23.40%。

 春雨教育同步作文系列答案
春雨教育同步作文系列答案【题目】(9分)掌握化学实验中常用仪器的特征和用途,有利于开展化学学习和研究。
(1)请从下列常见仪器图示中,选择恰当的字母序号填空
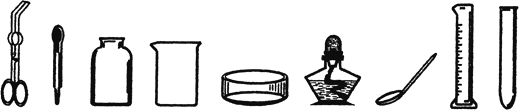
A B C D E F G H I
①可以直接在酒精灯火焰上加热的玻璃仪器是 ;
②镁条燃烧时,用来夹持镁条的仪器是 ;
③用酒精灯加热时需要垫上石棉网的仪器是 ;
④取用粉末状固体药品用到的仪器是 ;
⑤吸取和滴加少量液体试剂的仪器是 ;
⑥排空气法收集气体用到的玻璃仪器是 ;
(2)实验操作要规范化。下列操作中,正确的是 和 。(填序号)
A.点燃氢气、一氧化碳、甲烷等可燃性气体前,先检验气体纯度 |
B.用pH试纸测定溶液酸碱度时,先将pH试纸润湿,然后再测定 |
C.释然浓硫酸,将浓硫酸沿杯壁慢慢倒入盛水的烧杯中,并搅拌 |
D.用量筒量取一定量的液体时,仰视或俯视读数 |
(3)做化学实验要养成良好的整理习惯。若某同学在实验结束后,将仪器按下图放置,其中正确的一项是 。(填序号)
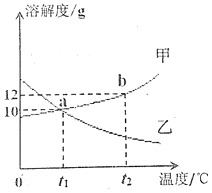
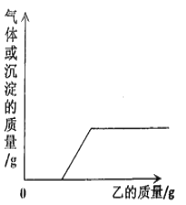
【题目】向下表的甲物质中逐滴加入相应的乙溶液至过量,反应过程中生成气体或沉淀的质量与加入乙的质量关系,能用下图图像表示的是
序号 | 甲 | 乙 |
① | HNO3和Mg(NO3)2的混合溶液 | KOH溶液 |
② | 银与锌的合金 | 稀H2SO4 |
③ | 久置空气中的铝片 | 稀HCl |
④ | 含有Na2CO3的NaOH溶液 | 稀HNO3 |
⑤ | HCl和H2SO4的混合酸 | Ba(NO3)2溶液 |
A. ②⑤ B. ①③⑤ C. ①②④ D. ①③④
【题目】某奶制品的营养成分见表:
项目 | 每100mL | NRV% |
能量 | 290kJ | 3% |
蛋白质 | 3.2g | 5% |
脂肪 | 4.0g | 7% |
碳水化合物 | 4.8g | 2% |
钠盐 | 62mg | 3% |
(1)________和水也是人体必需的基本营养物质,但在表中未标示.
(2)该奶制品中________能够提供能量(任写一种).
(3)奶制品中含有丰富的钙________(填“单质”、“原子”或“元素”),儿童每日要摄取足够量的钙,才能避免________(填字母序号). a.贫血症 b.佝偻病 c.甲状腺肿大
(4)如图是奶制品的两种包装.其中所使用的主要材料属于有机合成材料的是________(填字母序号,下同),属于无机合成材料的是________,应放入标有  的垃圾箱中的是________.
的垃圾箱中的是________.

(5)下列物质不会使蛋白质失去原有生理活性的是________(填字母序号).
a.浓硫酸 b.乙酸铅 c.硫酸铵 d.甲醛.