题目内容
已知:A是红色粉末,B、C是氧化物,D、I是常见金属,G为单质.它们之间的转化关系如下: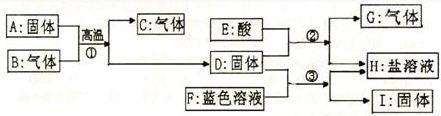
请回答:
(1)写出下列物质的化学式:A
(2)写出上述转化①②③中涉及到的化学方程式:
①
(3)为了安全,点燃G气体之前要
(4)分别用物理方法和化学方法从D和I的固体混合物除去固体D:
物理方法
化学方法

请回答:
(1)写出下列物质的化学式:A
Fe2O3
Fe2O3
、CCO2
CO2
、GH2
H2
.(2)写出上述转化①②③中涉及到的化学方程式:
①
Fe2O3+3CO
2Fe+3CO2
| ||
Fe2O3+3CO
2Fe+3CO2
;②
| ||
Fe+H2SO4=FeSO4+H2↑
Fe+H2SO4=FeSO4+H2↑
;③Fe+CuSO4=FeSO4+Cu
Fe+CuSO4=FeSO4+Cu
.属于置换反应的有②③
②③
.(3)为了安全,点燃G气体之前要
验纯
验纯
.(4)分别用物理方法和化学方法从D和I的固体混合物除去固体D:
物理方法
用磁铁吸引
用磁铁吸引
;化学方法
向其中加入过量的稀盐酸,直到无气泡产生为止
向其中加入过量的稀盐酸,直到无气泡产生为止
.分析:从已知:A是红色粉末,B、C是氧化物,AB高温下能生成金属单质D和气体C,所以A是氧化铁D是铁C是二氧化碳,据此为突破口对其他物质进行推断即可;
解答:解:从已知:A是红色粉末,B、C是氧化物,AB高温下能生成金属单质D和气体C,所以A是氧化铁D是铁C是二氧化碳,蓝色溶液F是硫酸铜的溶液,它能与铁反应生成硫酸亚铁和铜,所以H即为硫酸亚铁的溶液,I是铜,由于稀硫酸和铁反应能生成硫酸亚铁和氢气,所以G是氢气;
(1)由分析知ACG分别是氧化铁、二氧化碳和氢气,化学是为Fe2O3、CO2、H2;
(2)反应①是氧化铁和一氧化碳的反应产物是铁和二氧化碳,方程式为:Fe2O3+3CO
2Fe+3CO2;②是铁与稀硫酸的反应其产物是硫酸亚铁和氢气,方程式为Fe+H2SO4=FeSO4+H2↑;
③是铁和硫酸铜溶液的反应产物是铜和硫酸亚铁,方程式为:Fe+CuSO4=FeSO4+Cu;置换反应是单质与化合物反应生成另外的一种单质和一种化合物,分析以上三个反应可知②③是置换反应;
(3)G是氢气,氢气是可燃性气体,所以点燃G气体之前要验纯,以防止有爆炸产生;
(4)根据铁和铜中铁能被磁铁吸引,而铜不能,因此可以采用磁铁吸引的方式去除少量的铁;由于铁能与硫酸反应而铜不能,所以也可采用加入稀硫酸的方式去除铜中的铁;
故答案为:(1)Fe2O3;CO2;H2;
(2)Fe2O3+3CO
2Fe+3CO2;Fe+H2SO4=FeSO4+H2↑;Fe+CuSO4=FeSO4+Cu;②③;
(3)验纯;
(4)用磁铁吸引;向其中加入过量的稀盐酸,直到无气泡产生为止;
(1)由分析知ACG分别是氧化铁、二氧化碳和氢气,化学是为Fe2O3、CO2、H2;
(2)反应①是氧化铁和一氧化碳的反应产物是铁和二氧化碳,方程式为:Fe2O3+3CO
| ||
③是铁和硫酸铜溶液的反应产物是铜和硫酸亚铁,方程式为:Fe+CuSO4=FeSO4+Cu;置换反应是单质与化合物反应生成另外的一种单质和一种化合物,分析以上三个反应可知②③是置换反应;
(3)G是氢气,氢气是可燃性气体,所以点燃G气体之前要验纯,以防止有爆炸产生;
(4)根据铁和铜中铁能被磁铁吸引,而铜不能,因此可以采用磁铁吸引的方式去除少量的铁;由于铁能与硫酸反应而铜不能,所以也可采用加入稀硫酸的方式去除铜中的铁;
故答案为:(1)Fe2O3;CO2;H2;
(2)Fe2O3+3CO
| ||
(3)验纯;
(4)用磁铁吸引;向其中加入过量的稀盐酸,直到无气泡产生为止;
点评:根据图表中提供的信息再结合已学过的知识解这类题目时要先找出突破口再依此类推,从而得到问题的相关答案.

练习册系列答案
相关题目

 请回答:
请回答:
