题目内容
“三鹿奶粉事件”的“元凶”是三聚氰胺,其化学式为C3H6N6.三聚氰胺常被用作化工原料,微溶于水,有轻微毒性.三聚氰胺的相对分子质量是分析:根据三聚氰胺的化学式C3H6N6,及其化学式的表示意义,利用各元素的相对原子质量完成计算.
解答:解:
根据三聚氰胺的化学式C3H6N6,三聚氰胺的相对分子质量=12×3+1×6+14×6=126;其中碳、氢、氮原子的个数比=3:6:6=1:2:2;其中碳、氢、氮的元素质量比=(12×3):(1×6):(14×6)=6:1:14;252克三聚氰胺中氮元素质量=252g×
×100%=168g;
故答案为:126;1:2:2;6:1:14;168.
根据三聚氰胺的化学式C3H6N6,三聚氰胺的相对分子质量=12×3+1×6+14×6=126;其中碳、氢、氮原子的个数比=3:6:6=1:2:2;其中碳、氢、氮的元素质量比=(12×3):(1×6):(14×6)=6:1:14;252克三聚氰胺中氮元素质量=252g×
| 14×6 |
| 126 |
故答案为:126;1:2:2;6:1:14;168.
点评:根据化学式可以表示物质的组成与构成,利用化学式可判断物质的组成元素、可计算组成元素的质量比及质量分数等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
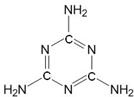 震惊全国的“三鹿奶粉”事件中的罪魁祸首是三聚氰胺(分子结构如图所示).三聚氰胺是一种重要的化工原料,由于其含氮量高,且目前国际上又通用“测氮法”标定牛奶中蛋白质含量,于是一些不法商人就将其混入奶粉中以“提高”奶粉的品质.
震惊全国的“三鹿奶粉”事件中的罪魁祸首是三聚氰胺(分子结构如图所示).三聚氰胺是一种重要的化工原料,由于其含氮量高,且目前国际上又通用“测氮法”标定牛奶中蛋白质含量,于是一些不法商人就将其混入奶粉中以“提高”奶粉的品质.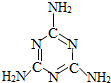 震惊全国的“三鹿奶粉”事件中的罪魁祸首是三聚氰胺(分子结构如图).三聚氰胺是一种重要的化工原料,由于其含氮量高,且目前国际上又通用“测氮法”标定牛奶中蛋白质含量,于是一些不法商人就将其混入奶粉中以“提高”奶粉的品质.
震惊全国的“三鹿奶粉”事件中的罪魁祸首是三聚氰胺(分子结构如图).三聚氰胺是一种重要的化工原料,由于其含氮量高,且目前国际上又通用“测氮法”标定牛奶中蛋白质含量,于是一些不法商人就将其混入奶粉中以“提高”奶粉的品质. (2009?河西区一模)震惊全国的“三鹿奶粉”事件中的罪魁祸首是三聚氰胺(分子结构如图).三聚氰胺是一种重要的化工原料,由于其含氮量高,且目前国际上又通用“测氮法”标定牛奶中蛋白质含量,于是一些不法商人就将其混入奶粉中以“提高”奶粉的品质.
(2009?河西区一模)震惊全国的“三鹿奶粉”事件中的罪魁祸首是三聚氰胺(分子结构如图).三聚氰胺是一种重要的化工原料,由于其含氮量高,且目前国际上又通用“测氮法”标定牛奶中蛋白质含量,于是一些不法商人就将其混入奶粉中以“提高”奶粉的品质. 震惊全国的“三鹿奶粉”事件中的罪魁祸首是三聚氰胺(分子结构如图所示).三聚氰胺是一种重要的化工原料,由于其含氮量高,且目前国际上又通用“测氮法”标定牛奶中蛋白质含量,于是一些不法商人就将其混入奶粉中以“提高”奶粉的品质.
震惊全国的“三鹿奶粉”事件中的罪魁祸首是三聚氰胺(分子结构如图所示).三聚氰胺是一种重要的化工原料,由于其含氮量高,且目前国际上又通用“测氮法”标定牛奶中蛋白质含量,于是一些不法商人就将其混入奶粉中以“提高”奶粉的品质.