题目内容
【题目】如图所示,三名由不同金属材料制成的“士兵”,要游过以下两片海域,完成获是银矿的任务。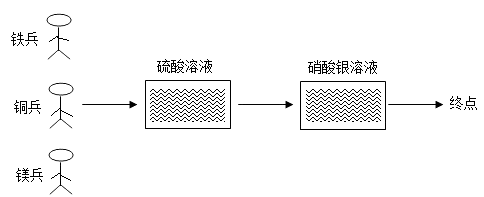
(1)最先牺牲的“士兵”是兵,用化学方程式解释:
(2)有一片“海域”最终会变成浅绿色,使它变色的“士兵”是兵。
(3)最终只有一名“士兵”完成任务,它是兵。
【答案】
(1)Mg;Mg +H2SO4= MgSO4 +H2↑
(2)Fe
(3)Cu
【解析】(1)三种金属的活动性顺序由强到弱为镁、铁、铜,所以镁先与硫酸反应;(2)铁发生置换反应时生成的亚铁盐溶液为浅绿色;(3)三种金属中铜不与硫酸发生反应,所以可以通过硫酸溶液与硝酸银溶液反应,置换出银,完成任务。根据金属活动性顺序的应用分析,在金属活动性顺序表中,排在氢前的金属能与酸发生反应,排在前面的金属能与排在后面的金属的盐溶液反应,根据反应是否发生也可证明金属的活动性的强弱。

练习册系列答案
相关题目
【题目】石灰厂为了测定一批石灰石样品中碳酸钙的质量分数,取用4g石灰石样品,把20g稀盐酸分4次加入样品中(样品中除碳酸钙外,其余的成分既不与盐酸反应,也不溶于水),充分反应后经过滤、干燥等操作,最后称量,得实验数据如下表:
实验次数 | 第一次 | 第二次 | 第三次 | 第四次 |
稀盐酸的用量 | 5g | 5g | 5g | 5g |
剩余固体的质量 | 3g | 2g | 1g | 1g |
(1)该石灰石样品中碳酸钙的质量分数是;
(2)计算该稀盐酸的溶质质量分数(写出计算过程,结果精确到0.1%).
(3)第三次加入5g稀盐酸后所得溶液的质量为 。