题目内容
【题目】铁的化合物有广泛用途,如碳酸亚铁(FeCO3)可作为补血剂,铁红(Fe2O3)可作为颜料,制备FeCO3和Fe2O3的一种流程如下图所示: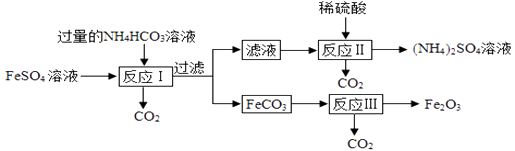
资料:FeCO3 ![]() FeO+CO2↑,4FeO+O2=2Fe2O3;
FeO+CO2↑,4FeO+O2=2Fe2O3;
FeSO4+2NH4HCO3=FeCO3↓+(NH4)2SO4+H2O+CO2↑
下列说法正确的是( )
A.反应Ⅰ需控制温度在35℃以下,原因可能是因为NH4HCO3受热易分解
B.滤液中的溶质只有( NH4)2 SO4
C.在空气中煅烧23.2g的FeCO3 , 得到Fe2O3和FeO的混合物15.2g。则生成Fe2O38.0g
D.在空气中充分煅烧FeCO3 , 若煅烧时间越多,则最终所得固体的质量越小
【答案】A,C
【解析】A. NH4H CO3受热易分解,因此反应Ⅰ需控制温度在35℃以下,否则硫酸亚铁不能与碳酸氢铵反应,A符合题意;
B. 滤液中的溶质有( NH4)2 SO4和过量的碳酸氢铵,B不符合题意;
C. 据质量守恒定律反应前后元素的种类质量不变,23.2g的FeCO3,铁元素的质量为23.2× ![]() =11.2g,同理可计算8gFe2O3中铁元素的质量为5.6g .7.2gFeO中铁元素为5.6g。即在空气中煅烧23.2g的FeCO3,得到Fe2O3和FeO的混合物15.2g。则生成Fe2O38.0g ,C符合题意;
=11.2g,同理可计算8gFe2O3中铁元素的质量为5.6g .7.2gFeO中铁元素为5.6g。即在空气中煅烧23.2g的FeCO3,得到Fe2O3和FeO的混合物15.2g。则生成Fe2O38.0g ,C符合题意;
D. 在空气中充分煅烧FeCO3,若煅烧时间越多,氧化亚铁转化成氧化铁越充分,则最终所得固体的质量越大,D不符合题意。
故答案为:AC。
根据流程图分析解答问题题,要注意分析各步骤中涉及到的物质及相关反应,分析判断,判断反应后物质成分时要注意除生成物外还要确定反应物是否有剩余。

练习册系列答案
相关题目