��Ŀ����
����Ŀ��ijѧУ��ѧ��ȤС��ͬѧ��ʵ���ҷ���һƿ���˸�ƿ�ǵ�NaOH���壬����ɷ��Ƿ�����Լ����ʳ̶Ȳ�������Ȥ��ͬѧ�����������²��룬����������ʵ��̽����
��������⣩��ƿNaOH������Ʒ�ijɷ���ʲô�أ�
���������룩����1��ֻ��NaOH ����2��ֻ��Na2CO3 ����3������NaOH��Na2CO3
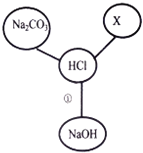
�����۽�����NaOH���ܱ��ʵ�ԭ����______���û�ѧ����ʽ��ʾ��
��ʵ��̽������1��ȡ������Ʒ���Թ��У���������ϡ���ᣬ�����ݲ�����˵������______��������
��2����һ����̽���������£�
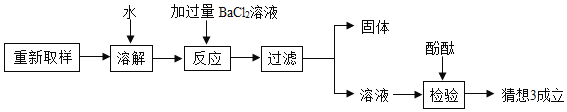
��������̽�����̻ش�
�ټ������BaCl2��Һ��������______��
�ڲ���������Ba��OH��2��Һ���������BaCl2��Һ��ԭ����______��
��������Һ�����������̪��Һ�������3��������______��
A CuCl2��Һ B KNO3��Һ C CaCl2��Һ D NH4Cl��Һ
��ʵ�鷴˼��ʵ�����NaOH����ı��淽����______��
���𰸡�2NaOH+CO2=Na2CO3+H2O 1 Ϊ��ʹ̼���Ƴ�ַ�Ӧ�� Ba��OH��2��Һ��̼���Ʒ�Ӧ������������ AD �ܷⱣ��
��������
[���۽���]�������ƺͶ�����̼��Ӧ����̼���ƺ�ˮ����Ӧ�Ļ�ѧ����ʽΪ��2NaOH+CO2=Na2CO3+H2O��
[ʵ��̽��]
��1��̼���κ����ᷴӦ�����ɶ�����̼��ȡ������Ʒ���Թ��У���������ϡ���ᣬ�����ݲ�����˵������1��������
��2����̼���ƺ��Ȼ�����Ӧ������̼�ᱵ�����ͺ��Ȼ��ƽ������Լ������BaCl2��Һ�������ǣ�Ϊ��ʹ̼���Ƴ�ַ�Ӧ����������������̼���Ʒ�Ӧ���������������ӣ����������Ƶļ�����ɸ��ţ����Բ���������Ba(OH)2 ��Һ���������BaCl2��Һ��ԭ���ǣ�Ba��OH��2��Һ��̼���Ʒ�Ӧ�����������ƣ�
���������ƺ��Ȼ�立�Ӧ�������д̼�����ζ�İ������Ȼ�ͭ������������Һ��Ӧ������ɫ������Ҳ���Եģ���KNO3��Һ��CaCl2��Һ������������Һ����Ӧ��������ѡ��AD��
[ʵ�鷴˼]���������ڿ��������ױ��ʣ�����Ӧ���ܷⱣ�档