题目内容
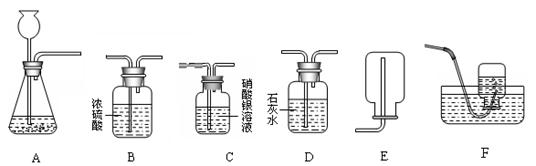
下图为实验室中常见的装置。试根据题目要求,回答下列问题:
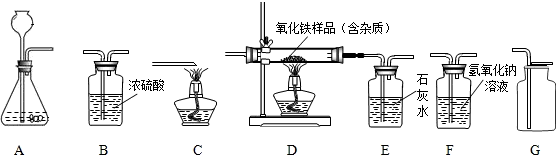
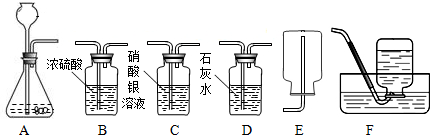
(1)以石灰石和稀盐酸为原料制取并收集干燥、纯净的二氧化碳(提示:盐酸中挥发出的少量HCl气体可用硝酸银溶液吸收)。
①所选装置的连接顺序为A→ (填写装置序号字母)。
②装置A中发生反应的化学方程式为 。
③装置B的作用是 。
④装置C中出现的现象为 。
(2)若用一氧化碳气体(含少量水蒸气)来测定某不纯氧化铁样品的纯度,气体流向是从左向右,选择的装置按B1→D→E→B2顺序连接,然后进行实验(假设有关反应均反应完全)。
①装置D中发生反应的化学方程式是 。
②对于上述设计的这个实验装置,你认为还需要改进的是 。
③通过测量反应前、后E洗气瓶的质量变化来计算氧化铁样品的纯度。若氢氧化钙溶液的量不足,则计算出样品纯度的结果将 (填“偏小”、“偏大”、“不受影响”之一)。
(1)CBH CaCO3+2HCl=CaCl2+H2O+CO2↑去除CO2中的水蒸气 有白色沉淀生成
(2)Fe2O3+3CO=2Fe+3CO2 添加尾气处理装置 偏小
【解析】
试题分析:(1)①由于要收集一瓶干燥、纯净的二氧化碳气体,就要把杂质氯化氢气体和水蒸气除去,由于氯化氢气体能与硝酸银溶液反应生成氯化银白色沉淀和硝酸,因此可以除去氯化氢气体,水蒸气可用浓硫酸除去,而且在除杂的过程中要后除去水,因为从硝酸银溶液中出来的气体中会含有水;因为要收集干燥的气体,且二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集,故连接顺序为CBH。
②实验室制取CO2,是在常温下,用石灰石和稀盐酸反应,生成氯化钙、水和二氧化碳,故装置A中发生反应的化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑。
③根据上面的分析可知,装置B的作用是去除CO2中的水蒸气。
④由于氯化氢气体能与硝酸银溶液反应生成氯化银白色沉淀和硝酸,故装置C中出现的现象是有白色沉淀生成。
(2)①一氧化碳具有还原性,在高温条件下,能与氧化铁反应,生成二氧化碳和铁,故装置D中发生反应的化学方程式是Fe2O3+3CO 2Fe+3CO2;
2Fe+3CO2;
②由于一氧化碳有毒性,若直接逸散到空气中,会对空气造成污染,故该装置需要添加尾气处理装置;
③根据题意,若氢氧化钙溶液的量不足,就不能完全吸收反应生成的二氧化碳,那么测量出来的二氧化碳的质量就会偏小,则通过二氧化碳计算出样品纯度的结果将会偏小。
考点:常用气体的发生装置和收集装置与选取方法,常见气体的检验与除杂方法,书写化学方程式,实验方案的设计与评价,根据化学方程式的计算
点评:此题是一综合性较强的实验设计题,涉及到多个知识点,有一定的难度,熟练掌握气体的制取装置和收集装置的选择、气体的检验、除杂等基础知识,是解题的关键,此外,还要能把握好实验数据的处理问题,以及实验方案的设计与评价问题。

 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案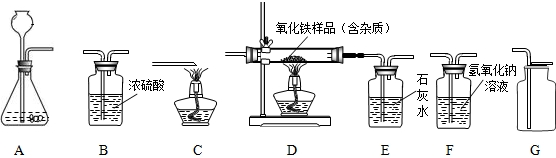

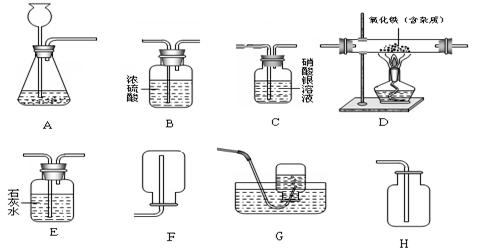
 (1)以金属锌和稀盐酸为原料制取并收集干燥、纯净的氢气(提示:盐酸中挥发出的少量HCl气体可用硝酸银溶液吸收)。
(1)以金属锌和稀盐酸为原料制取并收集干燥、纯净的氢气(提示:盐酸中挥发出的少量HCl气体可用硝酸银溶液吸收)。