题目内容
铜和铝是日常生活中常用的金属,金属钛是一种重要的航天金属材料,是21世纪最重要的金属之一.某学习小组对三种金属Ti、Al、Cu的金属活动性顺利进行探究.过程如下:
【提出假设】①Ti的金属活动性比Al强; ②Al的金属活动性比Cu强
【查阅资料】钛能与盐酸反应.
【实验设计】同温下,取大小厚薄相同的这三种金属片,分别投入等体积的足量的同种稀盐酸中,观察记录现象.
【操作分析】三种金属片在投入盐酸前都先用砂纸将表面擦光亮,其目的是 (填字母序号).
A、使表面光亮,便于观察
B、除去氧化膜,利于直接反应
C、使反应金属温度相同,易反应
【实验现象】
【实验结论】
(1)原假设中 不正确(填“①”或“②”)
(2)三种金属活动性由弱到强的顺序为 .
【结论应用】
(3)能否用铝制容器来盛装农药波尔多液(含硫酸铜), (填“能”或“否”),理由是 .
(4)2008年北京奥运会火炬的外形材料使用轻薄高品质铝合金的优点是
(任说出一点).
(5)钛和钛合金熔点高、密度小,抗腐蚀性能非常好,即使把它放在海水中数年,取出后仍光亮如初.因此被广泛用于火箭、航天飞机、船舶、化工和通信设备等.请写出钛的物理性质和化学性质各一条.
物理性质: ;
化学性质: .
【提出假设】①Ti的金属活动性比Al强; ②Al的金属活动性比Cu强
【查阅资料】钛能与盐酸反应.
【实验设计】同温下,取大小厚薄相同的这三种金属片,分别投入等体积的足量的同种稀盐酸中,观察记录现象.
【操作分析】三种金属片在投入盐酸前都先用砂纸将表面擦光亮,其目的是
A、使表面光亮,便于观察
B、除去氧化膜,利于直接反应
C、使反应金属温度相同,易反应
【实验现象】
| 金属 | Ti | Al | Cu |
| 与盐酸反应的现象 | 反应缓慢 | 反应剧烈 | 无明显现象 |
(1)原假设中
(2)三种金属活动性由弱到强的顺序为
【结论应用】
(3)能否用铝制容器来盛装农药波尔多液(含硫酸铜),
(4)2008年北京奥运会火炬的外形材料使用轻薄高品质铝合金的优点是
(任说出一点).
(5)钛和钛合金熔点高、密度小,抗腐蚀性能非常好,即使把它放在海水中数年,取出后仍光亮如初.因此被广泛用于火箭、航天飞机、船舶、化工和通信设备等.请写出钛的物理性质和化学性质各一条.
物理性质:
化学性质:
考点:金属活动性的探究,金属的物理性质及用途,书写化学方程式、文字表达式、电离方程式
专题:金属与金属材料
分析:【操作分析】根据题意本题是利用实验中的现象来探究金属的活泼性,由于金属放置在空气中易被氧化,所以实验前要打磨;
[实验结论]再根据金属与盐酸反应的快慢来判断金属的活泼性并写出反应的方程式;
【结论应用】
(3)根据金属的活泼性Al>Ti>Cu;所以铝制容器能与硫酸铜溶液反应并置换出铜解答;
(4)根据铝在空气中,表面易形成致密的氧化膜,起到保护作用.如耐腐蚀;铝的密度小,轻便解答;
(5)根据题中信息解答.
[实验结论]再根据金属与盐酸反应的快慢来判断金属的活泼性并写出反应的方程式;
【结论应用】
(3)根据金属的活泼性Al>Ti>Cu;所以铝制容器能与硫酸铜溶液反应并置换出铜解答;
(4)根据铝在空气中,表面易形成致密的氧化膜,起到保护作用.如耐腐蚀;铝的密度小,轻便解答;
(5)根据题中信息解答.
解答:解:
【操作分析】金属放置在空气中易被氧化,氧化物与盐酸反应生成水,不利于观察反应的剧烈程度,
故答案为:除去氧化膜,便于直接反应;
[实验结论](1)通过实验的现象可知Ti与盐酸反应不如Al与盐酸反应剧烈,所以假设a不成立;
(2)根据实验现象反应越剧烈金属越活泼,故选Al>Ti>Cu;
故答案为:(1)①(2)Al>Ti>Cu;
【结论应用】因为金属的活泼性Al>Ti>Cu;所以铝制容器能与硫酸铜溶液反应并置换出铜,因此不能用铝制容器盛放硫酸铜溶液,反应的方程式为:2Al+3CuSO4═Al2(SO4)3+3Cu.
故答案为:否 2Al+3CuSO4═Al2(SO4)3+3Cu.
(4)铝在空气中,表面易形成致密的氧化膜,起到保护作用.如耐腐蚀;铝的密度小,轻便;
(5)钛和钛合金熔点高、密度小属于物理性质,海水中数年,取出后仍光亮如初,说明钛的抗腐蚀性很强属于化学性质.
答案:
【操作分析】除去氧化膜,便于直接反应
[实验结论](1)①(2)Al>Ti>Cu
【结论应用】
(3)否 2Al+3CuSO4═Al2(SO4)3+3Cu
(4)耐腐蚀;轻便
(5)熔点高、密度小 钛的抗腐蚀性很强
【操作分析】金属放置在空气中易被氧化,氧化物与盐酸反应生成水,不利于观察反应的剧烈程度,
故答案为:除去氧化膜,便于直接反应;
[实验结论](1)通过实验的现象可知Ti与盐酸反应不如Al与盐酸反应剧烈,所以假设a不成立;
(2)根据实验现象反应越剧烈金属越活泼,故选Al>Ti>Cu;
故答案为:(1)①(2)Al>Ti>Cu;
【结论应用】因为金属的活泼性Al>Ti>Cu;所以铝制容器能与硫酸铜溶液反应并置换出铜,因此不能用铝制容器盛放硫酸铜溶液,反应的方程式为:2Al+3CuSO4═Al2(SO4)3+3Cu.
故答案为:否 2Al+3CuSO4═Al2(SO4)3+3Cu.
(4)铝在空气中,表面易形成致密的氧化膜,起到保护作用.如耐腐蚀;铝的密度小,轻便;
(5)钛和钛合金熔点高、密度小属于物理性质,海水中数年,取出后仍光亮如初,说明钛的抗腐蚀性很强属于化学性质.
答案:
【操作分析】除去氧化膜,便于直接反应
[实验结论](1)①(2)Al>Ti>Cu
【结论应用】
(3)否 2Al+3CuSO4═Al2(SO4)3+3Cu
(4)耐腐蚀;轻便
(5)熔点高、密度小 钛的抗腐蚀性很强
点评:本题虽是探究实验题,但考查的是金属的活泼性,借助金属与酸反应的现象来训练学生分析解决问题的能力,知识迁移的能力.源于教材的探究性题将成为考试的热点.

练习册系列答案
相关题目
 乙烯是制塑料的主要原料,其分子结构如图所示,下列关于乙烯的叙述正确的是( )
乙烯是制塑料的主要原料,其分子结构如图所示,下列关于乙烯的叙述正确的是( )| A、乙烯属于有机高分子化合物 |
| B、乙烯是由碳、氧两种元素组成的 |
| C、乙烯中碳、氢元素的质量比为6:1 |
| D、每个乙烯分子中含有28个质子 |
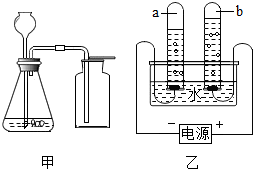 初中教材中可采用多种方法制取氧气.
初中教材中可采用多种方法制取氧气.