题目内容
在已调平衡的托盘天平两边各放一只等质量的烧杯,在两只烧杯里分别注入50g溶质质量分数为14.6%的稀盐酸,调至天平平衡后,向左边烧杯中加入2.4g金属Mg粉末,要使充分反应后天平仍然保持平衡,需向右边烧杯中加入CuO粉末的质量为( )A.2.2g
B.2.4g
C.3.2g
D.3.6g
【答案】分析:因为加入的盐酸质量相等,所以需要判断两端加入一定量物质后增加质量是否相等,增加质量相等时天平能仍然保持平衡,不相等时天平发生偏转.可根据化学方程式,借助关系式进行分析计算.
解答:解:设天平右边烧杯内加入金属镁后产生氢气的质量为x,由于左盘的物质全部保留的烧杯中,所以右盘的质量净增加也应该是2.2g,即加入的金属的质量应该是生成气体质量加2.2g;
Mg+2HCl=MgCl2+H2↑
24 73 2
2.4g 50g×14.6% x
方程式及各物质的量可知镁与盐酸恰好能够反应,故有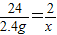
解得:x=0.2g; 即加入镁的烧杯质量增加2.4g-0.2g=2.2g;由于氧化铜和盐酸反应生成氯化铜和水,所以要使天平平衡则要加入氧化铜的质量是2.2g;
故选A
点评:加入物质充分反应后,天平一端增加的质量=加入固体质量-放出气体的质量,只有加入物质与放出气体质量均相等时,天平才能保持平衡.此题对于有关化学方程式的计算是否熟练是解题的关键.
解答:解:设天平右边烧杯内加入金属镁后产生氢气的质量为x,由于左盘的物质全部保留的烧杯中,所以右盘的质量净增加也应该是2.2g,即加入的金属的质量应该是生成气体质量加2.2g;
Mg+2HCl=MgCl2+H2↑
24 73 2
2.4g 50g×14.6% x
方程式及各物质的量可知镁与盐酸恰好能够反应,故有
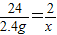
解得:x=0.2g; 即加入镁的烧杯质量增加2.4g-0.2g=2.2g;由于氧化铜和盐酸反应生成氯化铜和水,所以要使天平平衡则要加入氧化铜的质量是2.2g;
故选A
点评:加入物质充分反应后,天平一端增加的质量=加入固体质量-放出气体的质量,只有加入物质与放出气体质量均相等时,天平才能保持平衡.此题对于有关化学方程式的计算是否熟练是解题的关键.

练习册系列答案
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案
相关题目