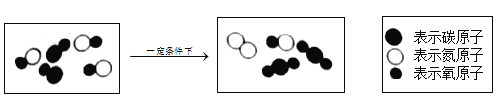
题目内容
【题目】实验员王老师要配制80克质量分数为10%的NaCl溶液供同学们使用,如图表示了他的实验操作过程。
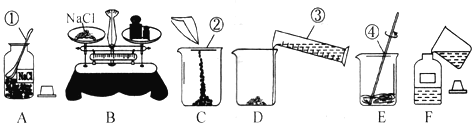
回答下列问题:
(1)写出标号①-④各仪器的名称。①_____②_____③_____④_____
(2)B操作中应称NaCl的质量是_____g,称量时若指针偏右,应进行的操作是_____;
(3)D操作中仪器③的规格应是_____(选填“50ml”或“100ml”),读数时应使视线与_____;
(4)E操作中④的作用是_____;
(5)下列错误操作可能导致溶质的质量分数偏小的是_____(填序号);
①B操作中砝码与NaCl放颠倒了 ②D操作中仰视凹液面最低处读数;
③D操作中有少量水溅出 ④F操作中溶液洒落。
(6)配制该溶液的正确步骤应是_____(填序号)。
【答案】药匙 烧杯 量筒 玻璃棒 8 增加左盘中的NaCl 100ml 凹液面的最低处保持水平 用于搅拌、加快NaCl溶解速率 ①② ABCDEF
【解析】
(1)①是药匙,②是烧杯,③是量筒,④是玻璃棒;
(2)氯化钠质量=80g×10%=8g,称量时若指针偏右,依据左物右码可知,氯化钠偏少,应进行的操作是增加左盘中的NaCl;
(3)量筒使用时,应采用就近原则,水的质量为80g-8g=72g,所以D操作中仪器③的规格应为100mL,读数时应使视线与凹液面的最低处保持水平;
(4)E操作的作用是:用于搅拌、加快NaCl溶解速率;
(5)质量分数偏小的可能原因是溶质少了或溶剂多了,所以
①B操作中砝码与NaCl放颠倒了,会使氯化钠质量减少,溶液质量分数偏小;
②D操作中仰视凹液面最低处读数,会使水质量增加,溶液质量分数偏小;
③D操作中有少量水濺出,是水质量较少,溶液质量分数偏大;
④F操作中溶液洒落,溶液具有均一性,不会影响溶质质量分数。故选:①②。
(6)称量食盐的质量首先打开广口瓶塞,倒放在桌面上,将取得的食盐放在天平的左盘,然后将称得的食盐放到烧杯中,再将量取的水倒入烧杯中,用玻璃棒搅拌使之溶解,配制该溶液的正确步骤应是ABCDEF;

 阅读快车系列答案
阅读快车系列答案【题目】某校课外小组同学用含有泥沙和氯化钠杂质的碳酸钠样品进行了如下实验:向一只60 g的烧杯中加入35 g样品,然后分5次加入盐酸,每次加入盐酸40 g(不考虑水、氯化氢逸出),每次反应完全后,称量烧杯和烧杯内物质的总质量。记录实验数据如下:
加入稀盐酸次数 | 1 | 2 | 3 | 4 | 5 |
烧杯和烧杯内物质的总质量/g | 132.8 | 170.6 | 208.4 | 246.2 | 286.2 |
已知:(1)第5次加酸后,烧杯底部剩余不溶固体2.1g。泥沙成分为SiO2,它不溶于水,也不与盐酸发生反应。
(2)![]()
请回答下列问题:
(1)反应过程中产生二氧化碳的总质量为_________。
(2)反应结束时得到氯化钠的质量_______ 。
(3)碳酸钠样品中钠元素与氯元素的质量比_________。
【题目】化学是一门以实验为基础的自然科学,化学实验和科学探究离不开装置。
制取气体的常用装置 |
A |
B |
C |
收集气体的常用装置 |
D |
E |
F |
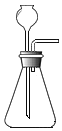
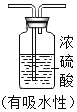
干燥气体的常用装置 |
G |
H |
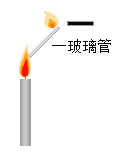
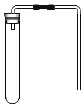
(1)制取气体时,首先要对发生装置进行气密性的检查,确保装置不漏气。检查装置C气密性的方法是:首先将导管的末端浸在水中,然后用双手紧握试管,一会儿发现导管末端_____,松开双手后,导管末端液面上升,形成一段稳定的水柱,说明装置的气密性良好。
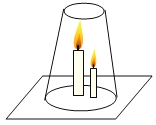
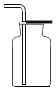
(2)收集气体的方法主要决定于气体的性质。装置F所示的收集方法是_____,被收集气体的密度_____空气的密度(填“大于”、“等于”或“小于”);如果用D装置收集某种气体,发现_____时,证明气体已集满。
(3)实验室用大理石和稀盐酸反应制取并收集一瓶干燥的二氧化碳气体,所选装置正确的连接顺序是_____→_____→_____(填装置编号)。
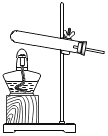
(4)从安全、环保、节能、简便等方面考虑,实验室制取氧气的最佳方法就是利用过氧化氢在二氧化锰做催化剂的条件下分解,其主要操作步骤有:①检查装置的气密性;②组装仪器;③向漏斗中注入过氧化氢溶液;④向维形瓶中放入二氧化锰;⑤收集气体。正确的操作顺序是_____(填序号)。
a.①②③④⑤ b.①④②③⑤ c.②①④③⑤ d.②③④①⑤
(5)写出用高锰酸钾加热制取氧气的化学方程式_____