题目内容
化学课上老师表演了一个小魔术——“无中生有”:相同条件下,向A、B两个体积相同的集气瓶中分别充满无色干燥的硫化氢(H2S)气体和二氧化硫气体。如图所示,抽开毛玻璃片,瓶口对紧,颠倒几次,使两种气体充分混合。一会儿,观察到两瓶内壁附着淡黄色固体颗粒,同时瓶壁上有小水珠出现。请根据现象回答下列问题:
(1)上述反应的化学方程式为_________________.
(2)如果这两个瓶子是质地较软的塑料瓶,会观察到 ,原因是_______。
(3)已知:相同条件下,相等体积的气体所含的分子数目相等。反应完毕,瓶中剩余的气体为____________(填化学式)。
 (1) 2H2S+SO2=3S+2H2O
(1) 2H2S+SO2=3S+2H2O
(2) 瓶子变瘪 气体消失气压减小 (3)SO2
解析试题分析:(1)上述反应是硫化氢与二氧化硫发生了反应,化学方程式为2H2S+SO2=3S+2H2O。
(2)如果这两个瓶子是质地较软的塑料瓶,会观察到瓶子变瘪;原因是气体消失,瓶内气压减小。
(3)由该反应的化学方程式可知,H2S和SO2反应时的个数比是2:1,故应完毕,瓶中剩余的气体为SO2。
考点:化学方程式的书写;化学反应现象;大气压;化学反应中各物质的微粒个数比。
点评:书写化学方程式要遵循客观事实和质量守恒定律两个原则,注意化学式要正确,不要忘记反应条件、气体或者沉淀符号。H2S和SO2反应时的配平系数分别是2和1,就是说H2S和SO2反应时的分子个数比是2:1。

练习册系列答案
 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案 名校名师培优作业本加核心试卷系列答案
名校名师培优作业本加核心试卷系列答案
相关题目
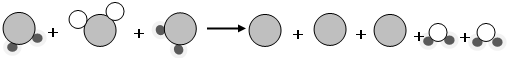
 ”表示氢原子,用“
”表示氢原子,用“ ”表示氧原子,用“
”表示氧原子,用“ ”表示硫原子,上述反应过程可用如图表示:
”表示硫原子,上述反应过程可用如图表示: