题目内容
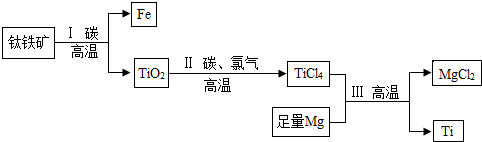
制造航空母舰使用大量合金材料(如铁合金、铜合金和钛合金等),钛(Ti)因其硬度大熔点高,常温下与酸和碱都不发生反应有很强的耐腐蚀性等优良性能被认为是本世纪重要的金属材料,由钛铁矿(主要成分是FeO和TiO2)提取金属钛的主要工艺流程如图:
①步骤Ⅰ中,发生的化学反应体现了碳的 性
②步骤Ⅱ中,TiO2、炭粉混合物在高温条件下通入氯气(Cl2)制得TiCl4和一种可燃性气体,该可燃性气体是 .
③步骤Ⅲ的反应方程式是 ,该反应需在氩气环境中进行,理由是 .所得金属钛中含有少量的金属镁.若要除去金属钛中的镁,可加入的试剂是 .充分反应后,再通过 (填操作名称)、洗涤、干燥即可.

①步骤Ⅰ中,发生的化学反应体现了碳的
②步骤Ⅱ中,TiO2、炭粉混合物在高温条件下通入氯气(Cl2)制得TiCl4和一种可燃性气体,该可燃性气体是
③步骤Ⅲ的反应方程式是
考点:物质的相互转化和制备,过滤的原理、方法及其应用,金属的化学性质,碳的化学性质,书写化学方程式、文字表达式、电离方程式
专题:物质的制备
分析:(1)根据碳参加的反应分析;
(2)根据质量守恒定律分析可燃性气体;
(3)根据流程分析步骤Ⅲ的反应写出反应的化学方程式,根据镁与酸反应,钛不能与酸反应,再通过过滤进行分离即可.
(2)根据质量守恒定律分析可燃性气体;
(3)根据流程分析步骤Ⅲ的反应写出反应的化学方程式,根据镁与酸反应,钛不能与酸反应,再通过过滤进行分离即可.
解答:解:(1)FeO和碳反应生成二氧化碳和铁,反应的化学方程式为:2FeO+C
CO2↑+2Fe,该反应中碳夺取了氧化亚铁中的氧,具有还原性.
(2)根据质量守恒定律可知反应前后元素种类不变,还缺少碳元素和氧元素,因为属于可燃性气体,所以是一氧化碳;
(3)由反应的流程可知,步骤Ⅲ的反应是四氯化钛与镁在高温条件反应生成氯化镁和钛,反应的方程式是:TiCl4+2Mg
2MgCl2+Ti;由于镁与酸反应,钛不能与酸反应,除去金属钛中的镁时,加入足量的稀盐酸或稀硫酸,反应完毕,过滤就可以除去镁,洗涤、干燥,得到纯钛金属.
故答为:①还原;②一氧化碳;③TiCl4+2Mg
2MgCl2+Ti,镁是比较活泼的金属.稀盐酸,过滤.
| ||
(2)根据质量守恒定律可知反应前后元素种类不变,还缺少碳元素和氧元素,因为属于可燃性气体,所以是一氧化碳;
(3)由反应的流程可知,步骤Ⅲ的反应是四氯化钛与镁在高温条件反应生成氯化镁和钛,反应的方程式是:TiCl4+2Mg
| ||
故答为:①还原;②一氧化碳;③TiCl4+2Mg
| ||
点评:解答本题关键是要熟悉金属活动性顺序,并能灵活运用解决实际问题,知道化学方程式的书写方法和注意事项.

练习册系列答案
 同步练习强化拓展系列答案
同步练习强化拓展系列答案
相关题目

 如图为浓盐酸的试剂瓶包装标签上的部分文字.请仔细阅读后回答以下问题:
如图为浓盐酸的试剂瓶包装标签上的部分文字.请仔细阅读后回答以下问题:
