题目内容
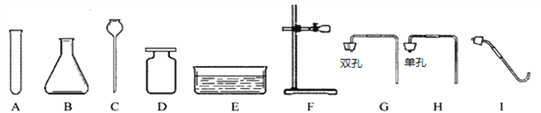
【题目】实验室常利用下列仪器进行气体的制取和性质实验,请回答:
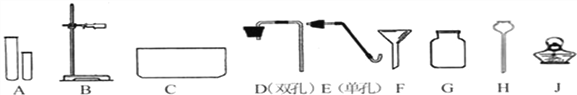
(1)写出仪器名称,H___________。
(2)实验室用高锰酸钾制取并收集纯净的氧气,应选择的仪器是________(填序号),反应的化学方程式是_______________。
(3)实验室要制取较多量的二氧化碳,装配气体发生装置时,应选择的仪器是_______(填序号)。小明同学把制取二氧化碳结束后的废液未经处理直接倒入下水道,可能造成的危害是 _______ (写一条)。
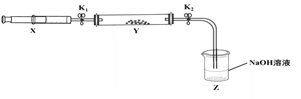
(4)利用下图装置进行实验(两玻璃管内径相同),实验前K1、K2、K3均已关闭。
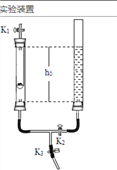
①左管燃烧匙装有足量的锌粒,右管盛有稀硫酸,打开K1、K2反应发生,方程式是_______________________,该装置的优点是________________,为使反应停止,操作是__________________。
②左管燃烧匙装有足量的白磷,右管盛水,光照引燃白磷,待白磷熄灭,冷却后,打开K2,右管液面下降,原因是______________________,至液面不在下降,右管液面高度为h1,计算空气中氧气体积分数的表达式为___________(用h0、h1表示)
【答案】 长颈漏斗 ABCEGJ 2KMnO4![]() K2MnO4+ MnO2+ O2↑ DGH 腐蚀铁质下水管道或污染水源等 Zn+ H2SO4 = ZnSO4 +H2↑ 控制反应的发生和停止 关闭K1 白磷消耗氧气,玻璃管内压强减少 (h0-h1)/h0×100%
K2MnO4+ MnO2+ O2↑ DGH 腐蚀铁质下水管道或污染水源等 Zn+ H2SO4 = ZnSO4 +H2↑ 控制反应的发生和停止 关闭K1 白磷消耗氧气,玻璃管内压强减少 (h0-h1)/h0×100%
【解析】(1)仪器H名称是长颈漏斗。(2)实验室用高锰酸钾制取并收集纯净的氧气,应选择的仪器是ABCEGJ,反应物是固体需加热制取气体,氧气不易溶于水,可以用排水法收集。反应的化学方程式是2KMnO4![]() K2MnO4+ MnO2+ O2↑。(3)实验室要制取较多量的二氧化碳,装配气体发生装置时,应选择的仪器是DGH,可以随时添加药品。把制取二氧化碳结束后的废液未经处理直接倒入下水道,可能造成的危害是腐蚀铁质下水管道或污染水源等,不可随意排放。(4) 利用下图装置进行实验。①左管燃烧匙装有足量的锌粒,右管盛有稀硫酸,打开K1、K2反应发生,方程式是Zn+ H2SO4 = ZnSO4 +H2↑,该装置的优点是控制反应的发生和停止。为使反应停止,操作是关闭K1,容器内气压增大,使两药品分离,反应停止。②左管燃烧匙装有足量的白磷,右管盛水,光照引燃白磷,待白磷熄灭,冷却后,打开K2,右管液面下降,原因是白磷消耗氧气,玻璃管内压强减少。至液面不在下降,右管液面高度为h1,计算空气中氧气体积分数的表达式为(h0-h1)/h0 ×100%。
K2MnO4+ MnO2+ O2↑。(3)实验室要制取较多量的二氧化碳,装配气体发生装置时,应选择的仪器是DGH,可以随时添加药品。把制取二氧化碳结束后的废液未经处理直接倒入下水道,可能造成的危害是腐蚀铁质下水管道或污染水源等,不可随意排放。(4) 利用下图装置进行实验。①左管燃烧匙装有足量的锌粒,右管盛有稀硫酸,打开K1、K2反应发生,方程式是Zn+ H2SO4 = ZnSO4 +H2↑,该装置的优点是控制反应的发生和停止。为使反应停止,操作是关闭K1,容器内气压增大,使两药品分离,反应停止。②左管燃烧匙装有足量的白磷,右管盛水,光照引燃白磷,待白磷熄灭,冷却后,打开K2,右管液面下降,原因是白磷消耗氧气,玻璃管内压强减少。至液面不在下降,右管液面高度为h1,计算空气中氧气体积分数的表达式为(h0-h1)/h0 ×100%。
点睛∶根据反应物状态和反应条件选择气体制取装置,根据生成物气体的溶解性和密度选择气体的收集方法。

【题目】材料是人类赖以生存和发展的重要物质,铜是目前使用最广泛的金属之一。
(一)铜材料的有关知识
(1)人类使用金属先后经历了“青铜”、“铁器”时代,直到近代才开始大量使用铝材料。这也反映出Cu、Fe、Al三种金属的活动性由强到弱的顺序是________。
(2)纯铜又称紫铜,常见铜合金有黄铜、青铜等种类。家用电缆常用紫铜,以聚氯乙烯塑料或TPU橡胶包裹。
① 以上叙述中不涉及到的材料是_______(选填序号)。
A.金属材料 B.无机非金属材料 C.有机合成材料
② 我国在西汉时期就有“曾青得铁则化为铜”之说,用化学方程式表示其原理_______。
③ 鉴别黄铜和黄金,以下方法不可行的是______(选填序号)。
A.观察颜色 B.加稀盐酸 C.在空气中灼烧
(二)铜及其化合物的实验
I.硫酸铜是制备其他含铜化合物的重要原料,以下是制取硫酸铜的常见方法。
(1)方案1:向稀硫酸中加入铜粉,再用导管通入空气并加热,铜粉逐渐减少,溶液由无色变为蓝色。
①反应中溶液的PH逐渐_________(填“增大”或“减小”)。
②该反应的化学方程式_________。
(2)方案2:将铜片加入浓硫酸中,加热,产生刺激性气味,溶液逐渐变成蓝色。将产生的气体通入酸性高锰酸钾溶液中,溶液褪色,说明该气体是________。
(3)从环保角度进行比较,你认为方案_______(填“1”或“2”)更合理。
Ⅱ.在一定量硫酸铜溶液中加入碳酸钠溶液,过滤、洗涤、低温干燥得到碱式碳酸铜固体,其组成为:xCuCO3·yCu(OH)2·zH2O。能证明固体已洗净的方法为__________。
(三)碱式碳酸铜的热分解实验
兴趣小组称取此固体12.0g,在科研人员的指导下用下图装置进行热分解实验。

【查阅资料】Cu(OH)2的分解温度为66℃~68℃,CuCO3的分解温度为200℃~220℃,各生成对应的两种氧化物。该碱式碳酸铜失去结晶水的温度与Cu(OH)2的分解温度接近。
(1)装置A的作用是___________。
(2)加热前后及过程中均通入空气,加热后通空气的目的是________。
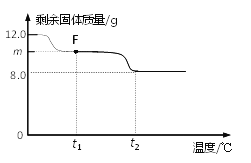
(3)控制温度在不同的范围对B中样品加热。测得装置C、D的质量在实验前后的变化情况如下表所示,测得B中剩余固体质量随温度的变化如下图所示。
装置 | 实验前/g | 实验后/g |
C | 198.0 | 199.8 |
D | 221.0 | 223.2 |
①图中F点对应的m=__________。
② 根据提供的数据, xCuCO3·yCu(OH)2·zH2O中x ﹕y ﹕z = _________。
③ 若缺少装置E,测得的________(选填“x”、“y”、“z”)的值会偏大。