题目内容
(14分)如图所示为实验室常用的实验装置,据此回答下列问题:
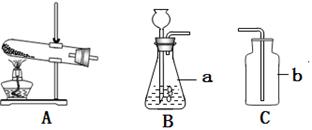
(1)写出标号所示仪器的名称b 。
(2)实验室用高锰酸钾制取氧气的反应表达式为 。
小明同学打算从制取O2后的固体残渣中回收二氧化锰(固体残渣中只有MnO2不溶于水)的方法是溶解、 、洗涤并干燥。
(3)收集二氧化碳只能用C装置的原因是 。
(4)小雯发现在加热硬水的过程中,产生了一种难溶性的固体。提出猜想: 难溶性的固体可能是碳酸钙。向这种难溶性的固体中滴入稀盐酸稀盐酸,观察到有大量的气泡产生,则这种固体可能是碳酸钙;若这种固体是碳酸钙,写出该反应的表达式 。
(5)如图是小雯用这种固体制取CO2,并验证CO2性质的实验组合装置,根据装置解答下列问题:

①方框中的发生装置应选择本题上右图中 (选填:A、B)装置;
②在装置D中可观察到的实验现象是:___ __,其相关的反应表达式为: ;
③装置E通常用于实验室检验CO2气体,现象是:________ _____________;
④装置F中可观察到奇妙的现象,从而说明CO2可用于:________ _____________;
⑤实验室要制取NO2气体做微粒运动的演示实验。NO2是一种红棕色的气体,密度比空气大,易被氢氧化钠溶液吸收,能与水反应生成硝酸和NO;NO2和NO都有毒,易污染环境。

Ⅰ.收集NO2可用如图1所示的装置, NO2应从端__ __(填“a”或“b”)通入。
Ⅱ.实验室通常在收集装置后还连接一套图2所示的装置,你认为这套装置的主要作用是:
Ⅲ.如图3,做微粒运动演示实验时,为缩短演示时间,NO2最好盛放在 (填“上”或“下”)面的集气瓶中,另一瓶放空气。抽去玻璃片可看到: 。

(1)写出标号所示仪器的名称b 。
(2)实验室用高锰酸钾制取氧气的反应表达式为 。
小明同学打算从制取O2后的固体残渣中回收二氧化锰(固体残渣中只有MnO2不溶于水)的方法是溶解、 、洗涤并干燥。
(3)收集二氧化碳只能用C装置的原因是 。
(4)小雯发现在加热硬水的过程中,产生了一种难溶性的固体。提出猜想: 难溶性的固体可能是碳酸钙。向这种难溶性的固体中滴入稀盐酸稀盐酸,观察到有大量的气泡产生,则这种固体可能是碳酸钙;若这种固体是碳酸钙,写出该反应的表达式 。
(5)如图是小雯用这种固体制取CO2,并验证CO2性质的实验组合装置,根据装置解答下列问题:

①方框中的发生装置应选择本题上右图中 (选填:A、B)装置;
②在装置D中可观察到的实验现象是:___ __,其相关的反应表达式为: ;
③装置E通常用于实验室检验CO2气体,现象是:________ _____________;
④装置F中可观察到奇妙的现象,从而说明CO2可用于:________ _____________;
⑤实验室要制取NO2气体做微粒运动的演示实验。NO2是一种红棕色的气体,密度比空气大,易被氢氧化钠溶液吸收,能与水反应生成硝酸和NO;NO2和NO都有毒,易污染环境。

Ⅰ.收集NO2可用如图1所示的装置, NO2应从端__ __(填“a”或“b”)通入。
Ⅱ.实验室通常在收集装置后还连接一套图2所示的装置,你认为这套装置的主要作用是:
Ⅲ.如图3,做微粒运动演示实验时,为缩短演示时间,NO2最好盛放在 (填“上”或“下”)面的集气瓶中,另一瓶放空气。抽去玻璃片可看到: 。
(1)b 集气瓶;
(2) KMnO4 K2MnO4 + MnO2 + O2; 过滤。
K2MnO4 + MnO2 + O2; 过滤。
(3) ρCO2﹥ρ空气且可溶于水。
(4) CaCO3+2HCl=CaCl2+H2O+ CO2↑
(5)①B ②变红,表达式为:H2O+CO2 =H2CO3
③变浑浊 ④灭火
⑤Ⅰ.a Ⅱ.防止NO2污染空气
Ⅲ.上 都变红(或两瓶气体变得一样红)
(2) KMnO4
 K2MnO4 + MnO2 + O2; 过滤。
K2MnO4 + MnO2 + O2; 过滤。(3) ρCO2﹥ρ空气且可溶于水。
(4) CaCO3+2HCl=CaCl2+H2O+ CO2↑
(5)①B ②变红,表达式为:H2O+CO2 =H2CO3
③变浑浊 ④灭火
⑤Ⅰ.a Ⅱ.防止NO2污染空气
Ⅲ.上 都变红(或两瓶气体变得一样红)
试题分析:(1)图中标号所示仪器的名称b:集气瓶;
(2)实验室用高锰酸钾制取氧气的反应表达式为2KMnO4
 K2MnO4 + MnO2 + O2↑;从制取O2后的固体残渣中回收二氧化锰(固体残渣中只有MnO2不溶于水)的方法是溶解、过滤、洗涤并干燥。
K2MnO4 + MnO2 + O2↑;从制取O2后的固体残渣中回收二氧化锰(固体残渣中只有MnO2不溶于水)的方法是溶解、过滤、洗涤并干燥。(3)收集二氧化碳只能用C装置的原因是ρCO2﹥ρ空气且可溶于水。
(4)碳酸钙固体中滴入稀盐酸稀盐酸反应的表达式为CaCO3+2HCl=CaCl2+H2O+ CO2↑;
(5)①制取二氧化碳是固体与液体反应,不要加热,故方框中的发生装置应选择本题上右图中的B。
②在装置D中可观察到的实验现象是:变红,其相关的反应表达式为H2O+CO2 =H2CO3;
③装置E通常用于实验室检验CO2气体,现象是:澄清石灰水变浑浊;
④装置F中可观察到奇妙的现象,从而说明CO2可用于:灭火;
⑤Ⅰ.NO2密度比空气大,故收集NO2可用如图1所示的装置, NO2应从端a通入;
Ⅱ.NO2和NO都有毒,易污染环境。实验室通常在收集装置后还连接一套图2所示的装置,这套装置的主要作用是防止NO2污染空气;
Ⅲ.如图3,做微粒运动演示实验时,为缩短演示时间,NO2最好盛放在上面的集气瓶中,另一瓶放空气。抽去玻璃片可看到:两瓶气体变得一样红。
点评:氧气和二氧化碳的制取是重要的知识点,对比学习,有利于掌握和拓展;
书写化学方程式要遵循客观事实和质量守恒定律两个原则,注意化学式要正确,不要忘记反应条件、气体或者沉淀符号。
二氧化碳能使澄清石灰水变浑浊,这个反应常用来检验二氧化碳。
紫色石蕊试液是酸碱指示剂,遇到酸性物质变红色,遇到碱性物质变蓝色。

练习册系列答案
 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案
相关题目






